【共同研究発表】網羅的な誘導体合成法を用いた新規抗菌薬リードの開発 ~薬剤耐性菌にも有効な新規抗菌薬開発への貢献に期待~

ポイント
・構造が複雑な天然物の誘導体を簡便かつ網羅的に合成する手法の開発に成功。
・新手法では、構造を変換した数百種類の誘導体を一挙に合成することが可能。
・薬剤耐性菌にも有効かつ新たな薬剤耐性を生じにくい新規誘導体を複数獲得。
<研究の概要>
北海道大学大学院薬学研究院の市川 聡教授、山本一貴助教、同大学大学院獣医学研究院の佐藤豊孝准教授、堀内基広教授、札幌医科大学の横田伸一教授、髙橋 聡教授、デューク大学薬学部のソクヨン リー教授、湧永製薬株式会社の風盛大地氏らの共同研究グループは、天然物誘導体の網羅的合成法と直接の生物活性評価を組み合わせた創薬プラットフォーム(in situビルドアップライブラリー法)を開発し、動物レベルでも有効な新規抗菌薬リード*1候補を開発しました。
既存薬が効かない細菌(薬剤耐性菌*2)の蔓延は世界的な問題ですが、新薬の開発は停滞しています。この状況が続けば、2025年には1,000万人の方が薬剤耐性菌による感染症で命を落とすとされ、新規抗薬剤耐性菌薬の開発は急務です。細菌の細胞壁の生合成を担うMraYを阻害する天然物は、薬剤耐性菌にも抗菌活性を示すことから、有望な新規抗菌薬リード候補として注目されています。しかし、抗菌活性・抗菌スペクトルは十分ではなく、そのままでは抗菌薬として用いることができません。そこで、これらの化学構造を改変する試みがなされていますが、その複雑な化学構造のため、化学構造を改変した誘導体の合成は容易ではなく、これらの天然物を基にした開発研究は滞っていました。
研究グループが開発したin situビルドアップライブラリー合成法では、複雑な化学構造を有する天然物の生物活性に重要な部分構造を有するコア化合物を用意し、構造が比較的単純なフラグメントとの連結により、大規模な誘導体群を簡便に合成することが可能です。この手法をMraY阻害天然物4種類に適用し、686個の誘導体を網羅的に合成することで、MraY阻害活性並びに抗菌活性が向上した誘導体を複数同定しました。さらに同定した高活性誘導体を基にさらなる構造改変を加えることで、in vivoモデルでも既存薬と同等以上の抗菌活性を示す誘導体を得ることに成功しました。本研究では、高活性誘導体とMraYとの複合体構造を、クライオ電子顕微鏡を用いて解明しました。これらの研究成果により、MraYを基にした抗菌薬開発に有用な知見をもたらし、新規抗菌薬開発の一助になることが期待できます。
さらにin situビルドアップライブラリー合成法は、抗がん活性を示すパクリタキセルなど3種類の天然物に適用し、585個の誘導体の合成と生物活性評価を短時間で達成しました。
なお本研究成果は、2024年6月14日(金)公開のNature Communications誌に掲載されました。
<背景>
抗菌薬が効かない細菌(薬剤耐性菌)の蔓延は世界的な問題ですが、新薬の開発コストの高騰だけでなく、開発してもすぐに薬剤耐性が生じてしまうため、また新薬開発の必要に迫られるなどの問題から、その開発は停滞しています。この状況が続けば、2025年には1,000万人が薬剤耐性菌による感染症で命を落とすとされ(この数字はがんで亡くなる方の数を超えると予想されます)、薬剤耐性菌にも有効な新規抗菌薬の開発が強く求められています。
細菌の細胞壁であるペプチドグリカン生合成を担う酵素の一つであるMraYを阻害する天然物は、薬剤耐性菌にも抗菌活性を示すことから、新規抗菌薬リード候補として注目されています。しかし、不十分な抗菌活性や細菌種への選択性、毒性などの問題により、そのままでは抗菌薬として用いることができません。そこで諸問題を解決するために、これらの化学構造を改変する試みがなされていますが、その複雑な化学構造のため、化学構造を改変した誘導体の合成は容易ではありません。また、MraY阻害剤が抗菌活性を発揮するためには、細菌の細胞膜を透過する必要があるものの、MraY阻害活性と細胞膜透過性の両方を考慮しながら、誘導体を設計することは大変難しいのが現状です。
<研究手法>
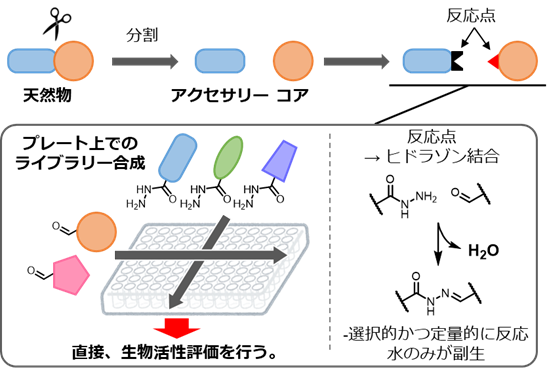
複雑な構造を有する天然物の化学構造と生物活性の迅速な最適化を達成すべく、天然物誘導体の網羅的合成法と直接の生物活性評価を組み合わせた創薬プラットフォーム(in situビルドアップライブラリー法)を開発しました(図1)。
本法では、まず天然物の化学構造を、標的との結合に重要なコアと、そのほかの機能にかかわるアクセサリーとに分けます。次に試薬を必要とせず、化学選択的かつ定量的に進行しうるような反応点をコアとアクセサリーに導入することで、両者を連結します。連結に使用する反応として、水のみを副生するヒドラゾン形成反応を用いました。アルデヒド部を有するコアと、ヒドラジン部を有するアクセサリーを混合するのみで誘導体を簡便に合成できます。
次に、この合成を生物活性評価に使用する96穴ウェルプレート上で一挙に行います。このプレートをそのまま生物活性を評価することができます。この方法により、簡便な操作で多数の誘導体を合成し、生物活性評価までシームレスに行うことが可能となります。網羅的に合成した誘導体のMraY阻害活性と抗菌活性を評価することで、迅速に新規創薬リード開発につなげられます。
<研究成果>
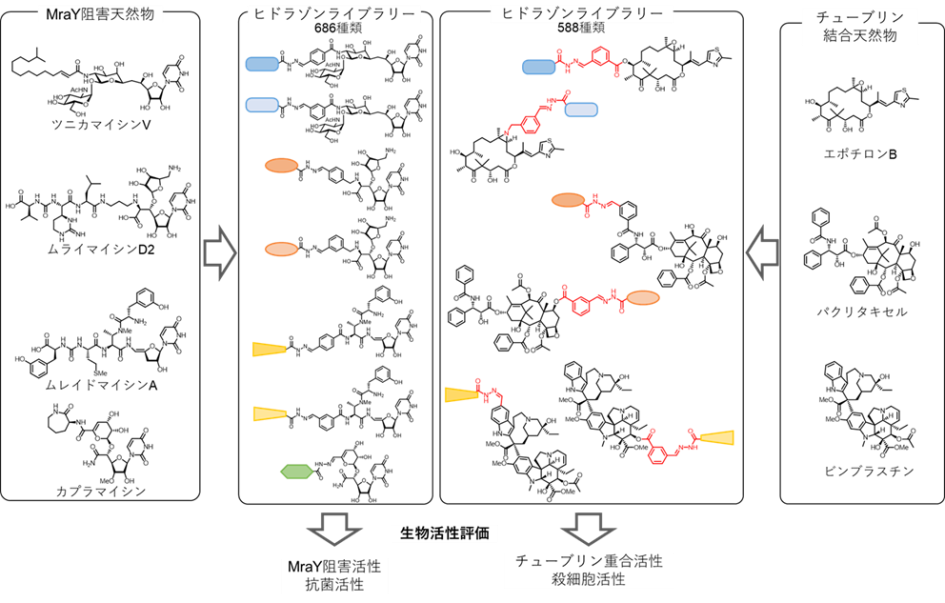
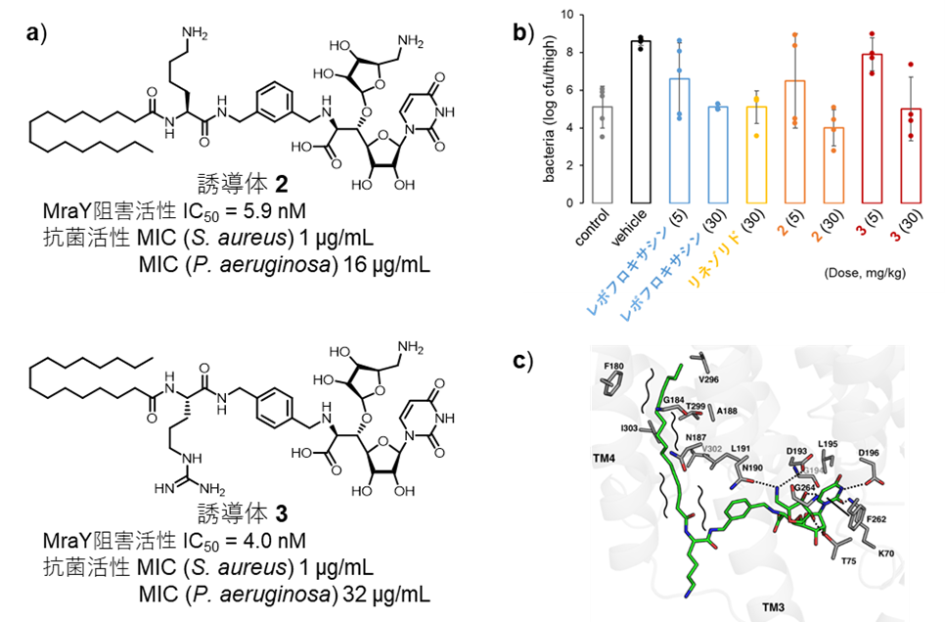
MraY阻害天然物として、ツニカマイシン、ムライマイシン、ムレイドマイシン、カプラマイシンの4種類を用い、in situビルドアップライブラリー合成法を適用することで、合計で686種の誘導体を一挙に合成しました(図2)。通常この規模の誘導体ライブラリー合成には、少なくとも数年を要するものの、この方法では、コアが用意できてしまえば1か月程度で合成を完了できました。この誘導体ライブラリーのMraY阻害活性と抗菌活性を評価することで、元の天然物よりもMraY阻害活性が向上したり、抗菌スペクトルが変化したりする誘導体を複数得ることができました。この誘導体のうち、抗菌活性が高いものを基にしてさらなる構造最適化*3を施すことで、MraY阻害活性が高く、グラム陽性菌並びにグラム陰性菌に抗菌活性を示す誘導体2と3を得ることができました(図3a)。誘導体2と3は、メチシリン耐性黄色ブドウ球菌(MRSA)やバンコマイシン耐性腸球菌(VRE)や、フルオロキノロンに耐性を持つ臨床分離株に対しても抗菌活性を示しました。さらにこれらの誘導体は、黄色ブドウ球菌マウス感染モデルにおいても、既存薬と同等以上の抗菌活性を示す事が分かりました。クライオ電子顕微鏡を用いて誘導体2並びに3とMraYとの複合体の立体構造も解明しており、この構造に基づいた論理的な薬物設計に使用できます。
in situビルドアップライブラリー合成法の一般性を検証すべく、抗がん活性を示すチューブリン重合調節活性を持つ天然物エポチロンB、パクリタキセル、ビンブラスチンにも本法を適用しました。本法を用いて、588種類の誘導体を合成し、チューブリン重合・脱重合活性が向上したり、殺細胞活性が向上したりした誘導体を得ることができました(図2)。
<今後への期待>
今回、得られた新規MraY阻害剤は、マウス感染モデルにおいても既存薬と同等以上の抗菌活性を示したことから、薬剤耐性菌に対抗するための新規抗菌薬リードとなることが期待できます。また、解明したMraYとの複合体構造を用いることでさらなる構造最適化も実施することができます。
また、今回確立したビルドアップライブラリー合成法は、化学構造も生物活性も全く異なるMraY阻害天然物とチューブリン結合天然物に適用できたため、構造が複雑な天然物や生理活性物質の網羅的な誘導体合成に汎用できることが期待され、中分子創薬の加速化への寄与も期待できます。
<謝辞>
本研究は、JSPS科研費JP22H02738、JP22K20704、JP21H03622、JP20H04757、AMED生命科学・創薬研究支援基盤事業JP22ama121039、AMED革新的先端研究開発支援事業JP23gm1610012、JP23gm1610013の助成を受けたものです。
<論文情報>
論文名 Development of a Natural Product Optimization Strategy for inhibitors against MraY,
a promising antibacterial target(天然物の構造最適化戦略による新規抗菌薬候補MraY
阻害剤の開発)
著者名 山本一貴1,2*、佐藤豊孝3,4,5、Aili Hao6、淺尾健太1、家口凜太郎1、日下慎太郎1、Radhakrishnam
Raju Ruddarraju 1、風盛大地7、瀬尾希来7、高橋 聡8,9、堀内基広3,4,5、横田伸一10、Seok-Yong Lee6、市川 聡1,2,11*(1北海道大学大学院薬学研究院、2北海道大学大学院薬学研究院創薬科学研究教育センター、3北海道大学大学院獣医学研究院、4北海道大学大学院国際感染症学院、5北海道大学 One Health リサーチセンター、6Department of Biochemistry, Duke University School of Medicine、7湧永製薬株式会社、8札幌医科大学付属病院、9札幌医科大学感染制御部、10札幌医科大学微生物学講座、11北海道大学国際連携研究教育局(GI-CoRE))*責任著者
雑誌名 Nature Communications(英国の科学論文総合誌)
DOI 10.1038/s41467-024-49484-7
公表日 2024年6月14日(金)(オンライン公開)
<参考図>
<用語解説>
*1 リード … 創薬開発研究の過程において、薬の有効成分である原薬となる分子が前臨床試験に進みうる分子であることを指す。ある疾患の治療標的タンパク質などに対して、その機能を制御できうる分子として見つかったものは「シード」と呼び、シードの構造最適化により「リード」へと至る。
*2 薬剤耐性菌 … 抗菌薬に対して抵抗性を示し、抗菌薬を処理しても死滅しない細菌のこと。複数の抗菌薬に抵抗性を示す場合は、多剤耐性菌と呼ばれ、治療が困難になる。
*3 構造最適化 … 分子の化学構造の一部を変化させることで、望みの機能を有する分子へと最適化していくこと。本研究の場合は、MraY阻害活性や抗菌活性、チューブリン結合活性や殺細胞活性を向上させることを指す。他にも毒性低減や代謝安定性改善などの諸性質も含まれる場合もある。
詳細は、下記のプレスリリース資料をご覧ください。
詳細は、下記のプレスリリース資料をご覧ください。