アジア人初の検証・日本単独の大規模治験を実施 — 潰瘍性大腸炎に対するオザニモドの有効性と安全性を実証 —
日本人潰瘍性大腸炎患者を対象としたS1P受容体調節剤 Ozanimodの大規模臨床治験(J-True North試験)を公表
~S1P receptor modulator as a new game exchanger of the treatment of ulcerative colitis ~
| 札幌医科大学医学部内科学講座 消化器内科学分野の仲瀬裕志教授と研究チームは、世界的に使用されている潰瘍性大腸炎治療薬「Ozanimod(オザニモド)」について、日本人患者198人を対象とした大規模臨床試験(J-True North試験)を実施し、その成果を発表しました。 本試験は日本単独で行われた新規薬剤治験であり、仲瀬教授が日本代表PI(研究プロジェクトの責任者)として全データを取りまとめました。研究チームは、この臨床試験によってオザニモドの有効性と安全性を日本人患者集団で初めて明確に示し、アジア人データとしても国際的に大きな意義を持つ成果を生み出しました。 |

<研究の概要>
スフィンゴシン1-リン酸(S1P)は、細胞増殖、分化、免疫等を調節する脂質メディエーターであり、5種のS1P受容体サブタイプのうち、リンパ球表面に高発現するS1P1受容体は、リンパ球がリンパ節等の二次リンパ組織から移出する過程で重要な役割を果たすことが知られています。Ozanimodは、S1P1とS1P5受容体に選択性を有し、特にリンパ球表面のS1P1に作用することで、リンパ球を末梢リンパ組織内に滞留させ、炎症部位へのリンパ球遊走を抑制すると考えられています。この薬剤は、米国で2020年3月に多発性硬化症、2021年5月に潰瘍性大腸炎(Ulcerative Colitis:UC)の治療薬として承認を取得しています。今回、日本人のUC患者のみを対象としたOzanimodの有効性および安全性の、国内第Ⅱ/Ⅲ相試験(RPC01-3103試験)[J-True North試験]が行われ、その有効性と安全性が2025年9月15日に、Gastro Hep Advances (米国消化器病学会関連雑誌)において掲載されました。
<研究のポイント>
スフィンゴシン1-リン酸(S1P)は、細胞増殖、分化、免疫等を調節する脂質メディエーターであり、5種のS1P受容体サブタイプのうち、リンパ球表面に高発現するS1P1受容体は、リンパ球がリンパ節等の二次リンパ組織から移出する過程で重要な役割を果たすことが知られています。Ozanimodは、S1P1とS1P5受容体に選択性を有し、特にリンパ球表面のS1P1に作用することで、リンパ球を末梢リンパ組織内に滞留させ、炎症部位へのリンパ球遊走を抑制すると考えられています。この薬剤は、米国で2020年3月に多発性硬化症、2021年5月に潰瘍性大腸炎(Ulcerative Colitis:UC)の治療薬として承認を取得しています。今回、日本人のUC患者のみを対象としたOzanimodの有効性および安全性の、国内第Ⅱ/Ⅲ相試験(RPC01-3103試験)[J-True North試験]が行われ、その有効性と安全性が2025年9月15日に、Gastro Hep Advances (米国消化器病学会関連雑誌)において掲載されました。
<研究のポイント>
- 日本人UC患者198人を対象としたOzanimodの有効性・安全性を検討しました。
- 炎症性腸疾患(IBD)分野においては、世界的に使用される薬剤を用いた日本人UC患者単独の臨床試験です。
- 実臨床に則した、treat through 観察研究の方法で治験が行われました。
- IBD専門医のご尽力により、198人の治験参加患者が得られたことは快挙であり、Ozanimodの十分な有効性および安全性の評価が日本人単独で可能となりました。
- アジア人におけるオザニモドの有効性と安全性が検証されたのは今回が初めてです。
- 国際治験はTrue North試験と命名されており、今回は日本単独の治験であり、J(Japan)-True North試験と名付けられました。
<研究の背景、実施期間など>
UCは炎症性腸疾患のひとつであり、日本において患者数が増加傾向にあります。主に大腸粘膜を直腸から連続性に侵し、しばしばびらんや潰瘍を形成するびまん性非特異性炎症です。その発症原因は未だに明らかとなっていません。UCの治療は、重症度や罹患範囲・QOLの状態等を考慮して、活動期には寛解導入治療を行い、寛解導入後は寛解維持治療を長期にわたり継続する必要があります。長期予後改善の観点から、粘膜治癒、さらには組織学的寛解を目指す戦略が提唱されています。また、患者さんの生活のスタイルに合った薬剤選択も重要となっています。
UCは炎症性腸疾患のひとつであり、日本において患者数が増加傾向にあります。主に大腸粘膜を直腸から連続性に侵し、しばしばびらんや潰瘍を形成するびまん性非特異性炎症です。その発症原因は未だに明らかとなっていません。UCの治療は、重症度や罹患範囲・QOLの状態等を考慮して、活動期には寛解導入治療を行い、寛解導入後は寛解維持治療を長期にわたり継続する必要があります。長期予後改善の観点から、粘膜治癒、さらには組織学的寛解を目指す戦略が提唱されています。また、患者さんの生活のスタイルに合った薬剤選択も重要となっています。
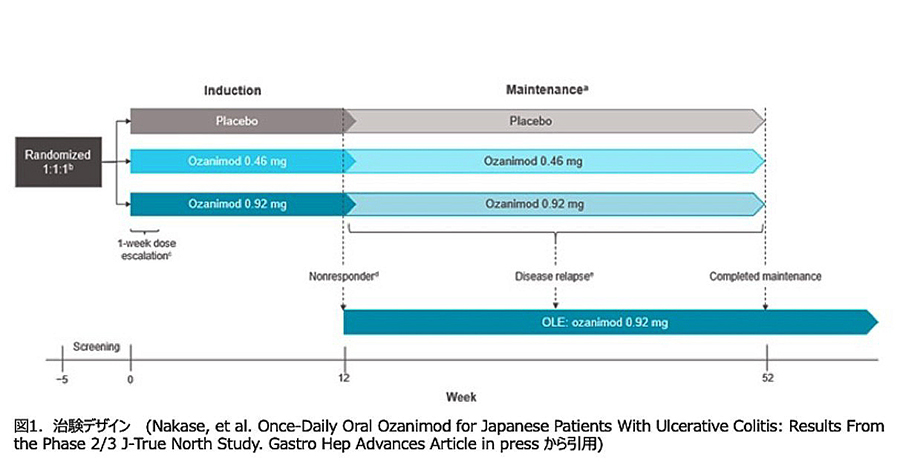
臨床治験の方法:2019年6月3日から2023年8月28日までに、日本人の中等症から重症のUC患者を対象として合計263名の患者が登録・スクリーニングされました。このうち198名が無作為化され、65名がプラセボ群、68名がオザニモド0.46mg群、65名がオザニモド0.92mg群に割り付けられています。今回の主要評価項目は、オザニモドのプラセボと比較した有効性を投与12週時点の臨床的改善によって検証するものです(図1)。
結果:オザニモド投与群では、プラセボ群と比較して、12週時点で臨床的反応を達成した患者の割合が有意に高かった(オザニモド0.46mg:52.9%、P=0.0158、オザニモド0.92mg:61.5%、P=0.0006、対プラセボ:32.3%)(図2)。
副次的評価項目においても同様の結果が認められ、オザニモド投与群はプラセボ群と比較して、12週時点で臨床的寛解、内視鏡的改善、粘膜治癒の達成率が高いことが示されました。有効性は全ての評価項目において52週目まで維持された。両用量のオザニモドは良好な忍容性を示し、寛解導入、維持期において予期せぬ安全性のシグナル(有害事象)は認められませんでした。
副次的評価項目においても同様の結果が認められ、オザニモド投与群はプラセボ群と比較して、12週時点で臨床的寛解、内視鏡的改善、粘膜治癒の達成率が高いことが示されました。有効性は全ての評価項目において52週目まで維持された。両用量のオザニモドは良好な忍容性を示し、寛解導入、維持期において予期せぬ安全性のシグナル(有害事象)は認められませんでした。
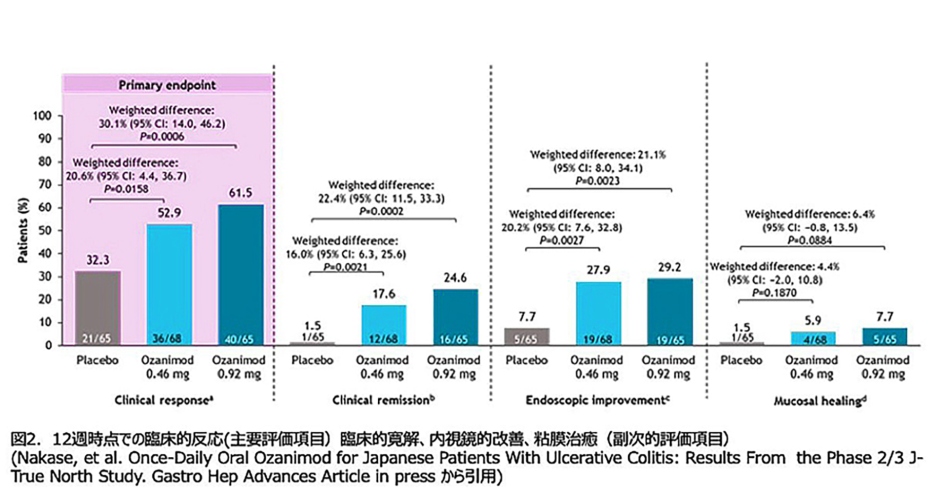
結論:この大規模臨床試験は、中等度から重度の活動性潰瘍性大腸炎を有する日本人患者において、1日1回経口投与のオザニモドの有効性と安全性を実証したと言えます。
<研究の意義、今後への期待>
世界的に使用される薬剤Ozanimodを用いて日本人UC患者単独での臨床試験を成し得たことは、海外へ大きなインパクトを与えました。UC患者の病態は多様性に富むため、様々な作用機序を有する薬剤の使用が可能となることは、患者にとって福音です。今後の課題として、OzanimodのUC 治療における位置付けです。長期の安全性については海外でのデータがすでに報告されていますが、日本における長期の安全性データ集積も必要となってきます。さらに、S1Pのシグナルが炎症性発癌に寄与するという基礎研究データがあり、Ozanimodによる炎症性発癌抑制効果について、今後の期待がかかっています。
世界的に使用される薬剤Ozanimodを用いて日本人UC患者単独での臨床試験を成し得たことは、海外へ大きなインパクトを与えました。UC患者の病態は多様性に富むため、様々な作用機序を有する薬剤の使用が可能となることは、患者にとって福音です。今後の課題として、OzanimodのUC 治療における位置付けです。長期の安全性については海外でのデータがすでに報告されていますが、日本における長期の安全性データ集積も必要となってきます。さらに、S1Pのシグナルが炎症性発癌に寄与するという基礎研究データがあり、Ozanimodによる炎症性発癌抑制効果について、今後の期待がかかっています。
<論文情報等>
詳細は、下記のプレスリリース資料をご覧ください。
- 論文名:Once-Daily Oral Ozanimod for Japanese Patients With Ulcerative Colitis: Results From the Phase 2/3 J-True North Study
- 掲載誌:Gastro Hep Advances
- URL: https://www.ghadvances.org/article/S2772-5723(25)00199-2/fulltext
- 著者:Hiroshi Nakase, Toshimitsu Fujii, Tadakazu Hisamatsu, Yasuo Suzuki, Mamoru, Watanabe, Sakuma Takahashi, Makoto Ooi, Ken Takeuchi, Tsuguhiro Kimura, Ken Furuya, Nobuo Aoyama, Kenkei Hasatani, Noriyuki Horiki, Kazunari Kanke, Satoki, Tokito, Souken Sai, Yoko Uchikawa, Shoichiro Goto, Go Fujimoto, Changliang Zhang, AnnKatrin Petersen, Toshifumi Hibi
- DOI: https://doi.org/10.1016/j.gastha.2025.100812
詳細は、下記のプレスリリース資料をご覧ください。