次世代抗がん治療の効き目を3D細胞培養技術で評価した論文が 国際科学誌「Acta Biomaterialia」に掲載
難治性がんの「バリア」を体外で再現し、「バリア」を打ち破る「薬剤候補」の特定に成功。 創薬支援事業への貢献を目指す
TOPPANホールディングス株式会社(本社:東京都文京区、代表取締役社長CEO:麿 秀晴、以下 TOPPANホールディングス)、国立大学法人大阪大学大学院工学研究科(以下、大阪大学)、公益財団法人がん研究会(以下、がん研究会)、および北海道公立大学法人札幌医科大学(以下、札幌医科大学)の4者は、これまで再現が難しかった、「難治性がん」が持つ、免疫細胞の攻撃を阻む強固な「バリア(物理的な障壁)」を、体外で再現した3Dモデルを構築することに成功しました。
近年主流となりつつあるがん免疫療法は、一部の難治性の固形がんが形成する強固な「バリア」によって、免疫細胞の攻撃が阻まれ、効果が限定的になることが最大の課題でした。このバリアは創薬の重要なターゲットですが、従来の技術では体外で再現し、評価に利用することが困難でした。
本研究では、TOPPANホールディングスが独自開発した3D細胞培養技術「invivoid®」を用い、細胞の位置を制御する事で難治性がんのバリアを体外で再現した3Dモデルを構築しました。このモデルで薬剤探索を行った結果、バリアを破壊し、免疫細胞によるがん細胞への攻撃力を大幅に高める「薬剤候補」の特定に成功しました。この成果は、難治性がんに対する革新的な創薬研究ひいては創薬支援事業への貢献が期待されます。
この度、本研究成果をまとめた論文が、バイオマテリアル分野を扱う国際科学誌「Acta Biomaterialia」に掲載されました。
近年主流となりつつあるがん免疫療法は、一部の難治性の固形がんが形成する強固な「バリア」によって、免疫細胞の攻撃が阻まれ、効果が限定的になることが最大の課題でした。このバリアは創薬の重要なターゲットですが、従来の技術では体外で再現し、評価に利用することが困難でした。
本研究では、TOPPANホールディングスが独自開発した3D細胞培養技術「invivoid®」を用い、細胞の位置を制御する事で難治性がんのバリアを体外で再現した3Dモデルを構築しました。このモデルで薬剤探索を行った結果、バリアを破壊し、免疫細胞によるがん細胞への攻撃力を大幅に高める「薬剤候補」の特定に成功しました。この成果は、難治性がんに対する革新的な創薬研究ひいては創薬支援事業への貢献が期待されます。
この度、本研究成果をまとめた論文が、バイオマテリアル分野を扱う国際科学誌「Acta Biomaterialia」に掲載されました。
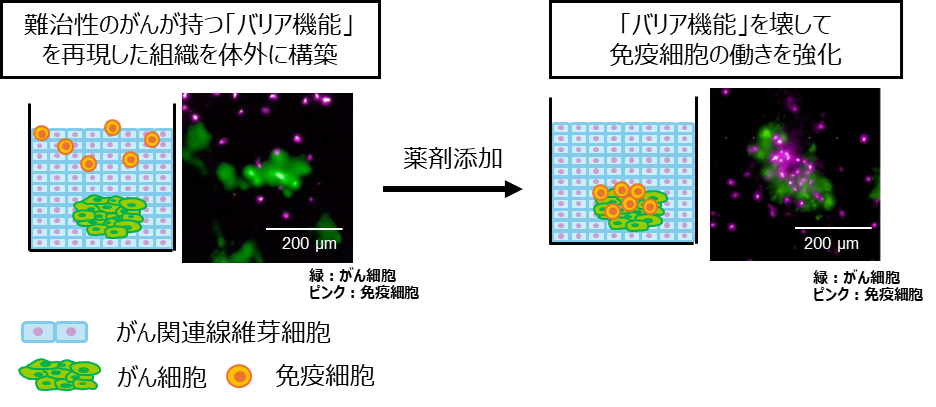
背景
近年、CAR-TやTCR-T(※1)をはじめとするがん免疫療法は目覚ましい進歩を遂げています。しかし一部の難治性の固形がんでは、T細胞(※2)が腫瘍内部に十分に侵入できず、治療効果が限定的であるという問題があります。T細胞の侵入を妨げる原因の一つは、がん関連線維芽細胞(CAF)などが大量のコラーゲンを産生し、物理的な障壁(バリア)を形成する免疫抑制性のがん微小環境(TME)の存在です。従来の細胞培養方法では、この複雑な空間構造や、CAFが生み出す強固なバリア機能を再現・評価することは困難でした。また免疫療法の評価には通常マウスが用いられていますが、マウスとヒトでは種差による免疫応答の違いがあるため、ヒトのがん微小環境をマウス体内で安定して再現出来ないという問題点があります。従って、ヒトの複雑ながん微小環境と免疫応答を体外で再現できる評価モデルが強く求められています。
本論文の概要
本研究ではTOPPANホールディングスらが独自に開発した3D細胞培養技術「invivoid®」を用いて、T細胞の動きやがん細胞の殺傷能力を定量的に評価できるモデルを構築しました。
①生体内の腫瘍微小環境を忠実に再現した構造の構築
本モデルは、間質細胞で層状構造を作り、その中にがん細胞の塊を持つという、ヒト生体内のTMEの特徴を模倣しています。T細胞を加えると、T細胞ががん細胞を認識して周りに集積しながら殺傷する現象が確認されました。
②難治性の固形がん特有の「免疫細胞排除」現象の体外での再現
線維芽細胞を活性化させ、CAFが豊富な間質組織(バリア)を構築しました。このモデルでは、T細胞の組織内部への侵入と、がん細胞の殺傷能力が著しく抑制され、免疫細胞を排除する難治性の固形がんの特性の再現に成功しました。
③強固な「バリア」を打ち破る薬剤候補の特定
この「免疫細胞が排除されるモデル」を利用して、バリア機能を低下させ、がん細胞の殺傷能力を回復させうる薬剤を約90種類の候補から探索しました。その結果、特定の薬剤であるヒストン脱アセチル化酵素(HDAC)阻害剤(※3)が、T細胞によるがん細胞の殺傷能力を大きく高める相乗効果を示すことが判明しました。この作用は、薬剤がCAFのバリア形成機能を弱めることで、T細胞の腫瘍内への侵入を促進するメカニズムを示唆しており、難治性の固形がんに対する新しい治療戦略につながる可能性があります。
①生体内の腫瘍微小環境を忠実に再現した構造の構築
本モデルは、間質細胞で層状構造を作り、その中にがん細胞の塊を持つという、ヒト生体内のTMEの特徴を模倣しています。T細胞を加えると、T細胞ががん細胞を認識して周りに集積しながら殺傷する現象が確認されました。
②難治性の固形がん特有の「免疫細胞排除」現象の体外での再現
線維芽細胞を活性化させ、CAFが豊富な間質組織(バリア)を構築しました。このモデルでは、T細胞の組織内部への侵入と、がん細胞の殺傷能力が著しく抑制され、免疫細胞を排除する難治性の固形がんの特性の再現に成功しました。
③強固な「バリア」を打ち破る薬剤候補の特定
この「免疫細胞が排除されるモデル」を利用して、バリア機能を低下させ、がん細胞の殺傷能力を回復させうる薬剤を約90種類の候補から探索しました。その結果、特定の薬剤であるヒストン脱アセチル化酵素(HDAC)阻害剤(※3)が、T細胞によるがん細胞の殺傷能力を大きく高める相乗効果を示すことが判明しました。この作用は、薬剤がCAFのバリア形成機能を弱めることで、T細胞の腫瘍内への侵入を促進するメカニズムを示唆しており、難治性の固形がんに対する新しい治療戦略につながる可能性があります。
4者の役割
・TOPPANホールディングス
独自の3D細胞培養技術「invivoid®」を用いた3D組織の作製と評価
・大阪大学
組織工学的観点から、「invivoid®」の改良・改善
・がん研究会
「バリア」を破壊する薬剤候補を探索するための薬物スクリーニング計画策定・実施
・札幌医科大学
研究全体の統括、およびTCR-Tや免疫細胞試料の提供
独自の3D細胞培養技術「invivoid®」を用いた3D組織の作製と評価
・大阪大学
組織工学的観点から、「invivoid®」の改良・改善
・がん研究会
「バリア」を破壊する薬剤候補を探索するための薬物スクリーニング計画策定・実施
・札幌医科大学
研究全体の統括、およびTCR-Tや免疫細胞試料の提供
論文掲載について
掲載誌: 「Acta Biomaterialia」
掲載日: 2025年10月15日
著者: 森村 吏惟、名田 イサナ、水江 由佳、篠崎 英司、藤田 直也、片山 量平、松﨑 典弥、廣橋 良彦★、北野 史朗★、鳥越 俊彦(★責任著者)
論文タイトル: Engineering a multilayered 3D stromal barrier model for quantitative analysis of T cell infiltration and cytotoxicity
掲載日: 2025年10月15日
著者: 森村 吏惟、名田 イサナ、水江 由佳、篠崎 英司、藤田 直也、片山 量平、松﨑 典弥、廣橋 良彦★、北野 史朗★、鳥越 俊彦(★責任著者)
論文タイトル: Engineering a multilayered 3D stromal barrier model for quantitative analysis of T cell infiltration and cytotoxicity
今後の展開
本研究で確立したモデルは、がん微小環境への免疫細胞の侵入を促進する新規薬剤の開発や、細胞間の相互作用メカニズムの解明に極めて有用です。
4者はこの技術を基盤とし、革新的な創薬研究や創薬支援事業への応用を加速します。
4者はこの技術を基盤とし、革新的な創薬研究や創薬支援事業への応用を加速します。
「invivoid®」について
大阪大学大学院工学研究科の松﨑 典弥教授とTOPPANホールディングスは、2017年4月より大阪大学大学院工学研究科に先端細胞制御化学(TOPPAN)共同研究講座を設置し、独自バイオマテリアルによる3D細胞培養技術に資する基礎研究を推進しています。「invivoid®」は生体に近い人工組織を簡便に作製できるため、がん個別化医療、薬効や毒性試験を含む創薬研究、再生医療、培養食料など幅広い用途が期待されています。
TOPPANホールディングスとがん研究会との共同ラボについて
019年2月よりがん研究会がん化学療法センター内に、TOPPANホールディングスと共同ラボを設置し、がん研究会の臨床的知見を得ながら、「invivoid®」による抗がん剤評価に資する臨床研究を推進しています。
※1 CAR-TやTCR-T:患者自身のT細胞を取り出し、がん細胞を認識・攻撃する能力を高めるように遺伝子を改変してから体内に戻す、次世代のがん免疫療法。
※2 T細胞:Tリンパ球とも呼ばれ、がん細胞などを直接攻撃して排除する免疫細胞。
※3 HDAC阻害剤:ヒストンの脱アセチル化を起こす酵素を阻害する事により、ヒストンのアセチル化を保持する事で作用する薬剤。HDAC 阻害薬の一つであるVorinostatは、皮膚 T 細胞リンパ腫に対して保険適応が認められている。
*本ニュースリリースに記載された商品・サービス名は各社の商標または登録商標です。
*本ニュースリリースに記載された内容は発表日現在のものです。その後予告なしに変更されることがあります。
※2 T細胞:Tリンパ球とも呼ばれ、がん細胞などを直接攻撃して排除する免疫細胞。
※3 HDAC阻害剤:ヒストンの脱アセチル化を起こす酵素を阻害する事により、ヒストンのアセチル化を保持する事で作用する薬剤。HDAC 阻害薬の一つであるVorinostatは、皮膚 T 細胞リンパ腫に対して保険適応が認められている。
*本ニュースリリースに記載された商品・サービス名は各社の商標または登録商標です。
*本ニュースリリースに記載された内容は発表日現在のものです。その後予告なしに変更されることがあります。
詳細は、下記のプレスリリース資料をご覧ください。