【共同研究成果】構造最適化に適した新たなペプチドスキャニング法の開発~ペプチド創薬への貢献に期待~ (北海道大学及び本学医学部微生物学講座 横田伸一教授、感染制御・臨床検査医学講座 髙橋 聡教授)
2023年2月2日
北海道大学
札幌医科大学
北海道大学
札幌医科大学
【ポイント】
・ペプチドの構造最適化の工程を大幅に削減できる新規スキャニング法の開発に成功。
・新手法では、アラニンスキャニング法では見出すことのできない部位に対する構造修飾が可能。
・薬剤耐性菌に有効な誘導体や様々な抗菌スペクトルを示す誘導体の獲得に成功。
【概要】
北海道大学大学院薬学研究院及び国際連携研究教育局バイオサーフィス創薬グローバルステーション(以下、GI-CoRE GSD)の市川 聡教授、勝山 彬助教、同大学大学院獣医学研究院の佐藤豊孝准教授、堀内基広教授、札幌医科大学の横田伸一教授、髙橋 聡教授らの共同研究グループは、ペプチドの創薬展開を迅速に実現できる新たなペプチドスキャニング法*1を開発しました。
近年の医薬品開発においては、新薬の種としてペプチドが注目されています。ペプチドを医薬品として開発する方法として、ペプチドスキャニング法を用いて、ペプチドの構造修飾を行う手法が知られています。この構造修飾は二段階に分けて行われますが、二段階目では、目的のペプチドを一から作り直す必要があり、この簡素化が求められていました。
研究グループが開発した方法は、ペプチド中の活性に重要な部分の同定と、その部分に対する構造修飾をシームレスに実行することができるうえ、生物活性評価直前での化学合成と組み合わせることで、数百の誘導体の一挙合成も可能です。また、本研究で開発した方法を抗菌ペプチド系天然物に用いることで、薬剤耐性菌に有効な誘導体や、元々の天然物とは異なる抗菌スペクトルを示す誘導体を獲得することに成功しました。これまでのペプチド創薬研究では、構造最適化のために数多くの試行錯誤が必要でした。本研究は、この構造最適化の工程を大幅に削減できることから、新規ペプチド医薬品を開発する方法の一つとして広く活用できると期待できます。
なお、本研究成果は、2023年1月28日(土)にJournal of the American Chemical Society誌にオンライン掲載されました。
【背景】
これまでの創薬化学研究においては、低分子化合物が医薬品候補として主たる役割を果たしてきました。これにより様々な疾患の治療が可能になりましたが、未だ治療法のない疾患も残されています。こうした中、近年では、低分子化合物では作用するのが難しい標的に対する医薬品の開発が重要な課題となっています。ペプチドは多数の相互作用を広い面で形成できる特徴があることから、こうした標的に効果的に作用できる分子として、その重要性が年々増してきています。
ペプチドを医薬品として開発していくためには、活性の向上や代謝安定性等の性質の改善が必要であり、このためにペプチドの構造修飾が行われます。この過程では、ペプチドスキャニングと呼ばれる系統的な手法によりペプチド中の変換可能なアミノ酸を同定した後、当該部位への適切な置換基*2の導入が行われます。一段回目においてはアラニンスキャニングをはじめとした優れた方法が知られていますが、二段階目の置換基導入に際しては目的のペプチドを一から作り直す必要があり、多大な労力が必要でした。
【研究手法】
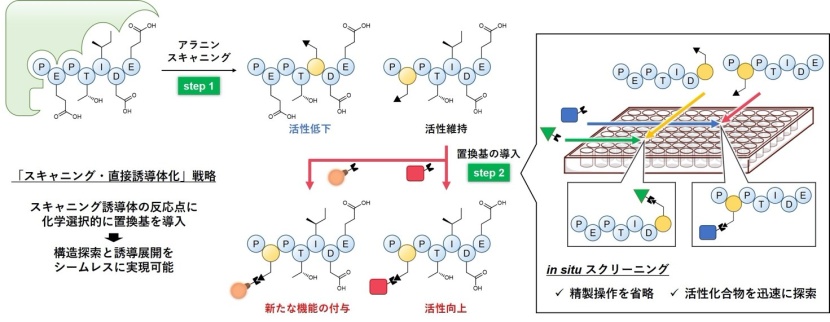
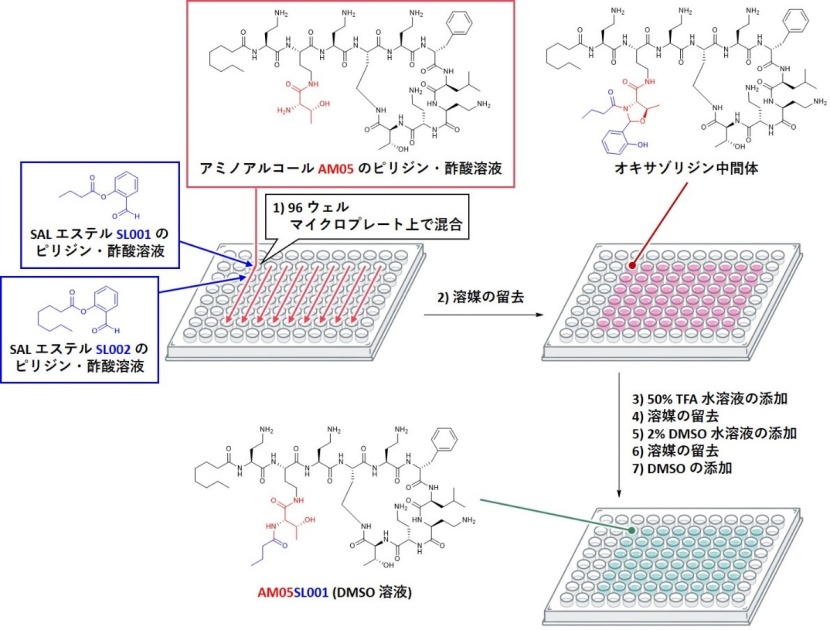
ペプチドスキャニングに用いるアミノ酸として、後の官能基導入の足がかりとなるアミノアルコールを有するアミノ酸を設計しました。このアミノアルコールに対しては、セリン/スレオニンライゲーション(STL)を用いることで、置換基の選択的な導入が可能です。このアミノ酸を用いたペプチドスキャニングを行ったのち、用いた無保護のスキャニング誘導体に対して、STLにより直接置換基を導入します。この際、生物活性評価直前に化合物を微量合成する手法(in situ化学*3)を併用することで、ペプチドスキャニング後の誘導体合成と生物活性評価をシームレスに行います(図1)。
【研究成果】
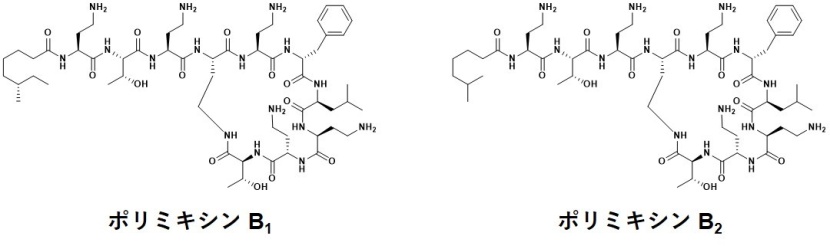
新たなペプチドスキャニングの手法を抗菌天然物であるポリミキシンB(図2)に適用し、その有用性を調査しました。スキャニング用のアミノ酸としてスレオニルジアミノブタン酸を用いるとともに、ポリミキシンの側鎖の長さについても同様に調査しました。
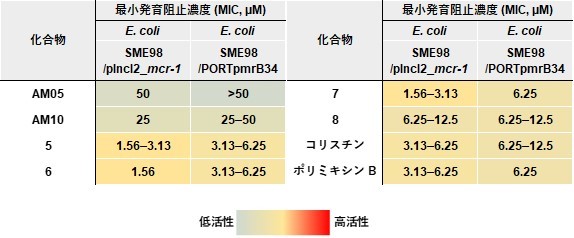
まず、アミノアルコール部位を有するスキャニング用誘導体に対する置換基導入と、続く抗菌活性評価について検討したところ、この2段階が極微量の検体を用いてシームレスに実施できることがわかりました。2種類の薬剤耐性菌に対するペプチドスキャニングの結果から、ポリミキシンBの3箇所に置換基導入が可能であることが分かりました。この部位に対して、STLを用いて様々な置換基を導入した結果、天然物と同等以上の活性を示す誘導体を複数獲得しました(図3)。
また、同様の手法を用いて9種類の細菌に対する抗菌活性の最適化を試みたところ、天然物よりも狭い抗菌スペクトルを有する誘導体や、反対に広範な抗菌スペクトルを有する誘導体も獲得することができました。また、ペプチドスキャニング法の代表的な例であるアラニンスキャニング法と本手法を比較することで、アラニンスキャニング法では見出すことのできない部位に対する構造修飾が可能であることが分かりました。
【今後への期待】
今回開発したペプチドスキャニング手法は、ポリミキシンBにとどまらず、ペプチド一般に応用可能です。この手法を様々なペプチドに対して適用することで、ペプチドの構造最適化を迅速に行うことができ、優れた生物活性を示す誘導体を獲得することができます。この方法を活用していくことで、ペプチドという創薬モダリティを用いた新規医薬品の開発に繋がることが期待されます。
【論文情報】
論文名 Discovery of Structurally Optimized Polymyxin Derivatives Facilitated by Peptide Scanning and In Situ Screening Chemistry
(ペプチドスキャニングとin situスクリーニング化学を用いたポリミキシンBの構造最適化)
(ペプチドスキャニングとin situスクリーニング化学を用いたポリミキシンBの構造最適化)
著者名 家口凜太郎¹、勝山 彬¹,²,³*、佐藤豊孝⁴,⁵,⁶、髙橋 聡⁷,⁸、堀内基広⁴,⁵,⁶、横田伸一⁷、市川 聡¹,²,³*(¹北海道大学大学院生
命科学院、²北海道大学大学院薬学研究院、³ GI-Core GSD、⁴北海道大学大学院獣医学研究院、⁵北海道大学大学院国際感染症学院、
⁶北海道大学 One Health リサーチセンター、⁷札幌医科大学、⁸札幌医科大学附属病院)
命科学院、²北海道大学大学院薬学研究院、³ GI-Core GSD、⁴北海道大学大学院獣医学研究院、⁵北海道大学大学院国際感染症学院、
⁶北海道大学 One Health リサーチセンター、⁷札幌医科大学、⁸札幌医科大学附属病院)
雑誌名 Journal of the American Chemical Society(化学の専門誌)
DOI 10.1021/jacs.2c12971.
公表日 2023年1月28日(土)(オンライン公開)
【参考図】
【用語解説】
*1 ペプチドスキャニング法 … アミノ酸が連なった分子であるペプチドの各アミノ酸残基を系統的に変化させることで、元のアミノ酸の生物
活性に対する寄与を調査する手法。このなかで、アミノ酸の一つであるアラニンを用いて置き換えていく方法をアラニンスキャニングと呼
ぶ。
活性に対する寄与を調査する手法。このなかで、アミノ酸の一つであるアラニンを用いて置き換えていく方法をアラニンスキャニングと呼
ぶ。
*2 置換基 … 複数の原子で構成されたひとまとまりの集合体。創薬化学においては、この様々な種類の置換基を元の分子に組み込むことで、
医薬品としての性質の改良を図ることが多い。
医薬品としての性質の改良を図ることが多い。
*3 in situ化学 … 「in situ」は「その場で」を意味し、創薬化学においては化学合成を生物活性評価直前に行う手法を指す。一般的に、化学
合成と生物活性評価は実験設備も異なる独立した実験である。これに対し、今回のin situ化学では、生物活性を行う設備・装置を用いて化学
合成を実施し、そのまま生物活性を評価することで、この二段階を迅速に行うことができる。
合成と生物活性評価は実験設備も異なる独立した実験である。これに対し、今回のin situ化学では、生物活性を行う設備・装置を用いて化学
合成を実施し、そのまま生物活性を評価することで、この二段階を迅速に行うことができる。