

私たちは皮膚のあらゆる病気を診療の対象とし、毛、爪、口腔粘膜、外陰部の病気も取り扱っています。全道の基幹病院や個人開業医院から多くの紹介患者さんが受診されており、地域の医療機関と協力しながら最善の医療を提供するように努めています。
● 対応疾患
皮膚・粘膜疾患全般。特に、悪性黒色腫を含む皮膚悪性腫瘍、アトピー性皮膚炎、アレルギー性疾患、遺伝性皮膚疾患を専門としています。診療にあたっては日本皮膚科学会や国内・国際学会で推奨されている診断基準や治療指針に則っています。
● 新患外来
受付時間:月・水・木・金曜日の午前8:45~午前11:00
2026年5月1日よりシステムが変更になり、他病院からの紹介状がない方は受け付けておりません。お薬手帳や、これまでの病名・治療歴などがわかるものをお持ちでしたら、持参してください。できるだけ待ち時間が少なくなるよう配慮しておりますが、混雑状況によってはお待ちいただく場合がございます。お時間に余裕を持ってご来院ください。
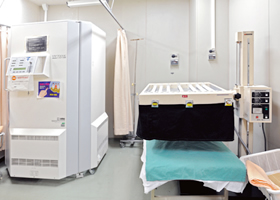
● 外来に設置している治療機器
・紫外線治療装置 (ナローバンドUVB、UVA、エキシマライト)
対象疾患:乾癬、菌状息肉症、尋常性白斑
・色素レーザー (V-beam)
対象疾患:赤アザ (血管腫)
・Qスイッチ付きアレキサンドライトレーザー (Alex)
対象疾患:青アザ (異所性蒙古斑、太田母斑)、茶アザ (扁平母斑)
・ノーマル発振アレキサンドライトレーザー (GentleLASE)
対象疾患:毛包関連疾患
・炭酸ガスレーザー
小手術に使用

【皮膚遺伝外来】
担当医:肥田時征
診療日時:毎週木曜日午後14:00-16:00
受診方法:皮膚科外来受診時に予約を入れます。電話予約はできませんのでご了承ください。他の医療機関からのご紹介の場合は、当院の地域医療連携室を通じてご連絡いただけますとスムーズです。
診療内容:遺伝性、先天性の皮膚疾患の診断、治療、皮膚ケアを担当します。患者さんご本人の状況、ご家族の状況など詳しくお聴きし、皮膚の状態を診察します。疾患に関する医学的な情報をご説明し、診断方法や治療方法を詳しくご説明いたします。また、遺伝に関するご相談をお受けいたします。初めて受診なさる場合には、過去の検査、診断の状況が分かる資料がありましたらご持参ください。
現在、当科で募集している治験一覧です。
当科はJCOG(日本臨床腫瘍研究グループ:国立がん研究センターがん研究開発費研究班を中心とする共同研究グループ)の皮膚腫瘍グループの参加施設です。
治験への参加を希望されている患者さまは、まずは「治験について」をご覧ください。
① 高リスク皮膚有棘細胞癌患者を対象に、手術及び放射線療法後のCEMIPLIMABによる補助療法とプラセボとを比較する無作為化、プラセボ対照、二重盲検試験(募集中)
試験験の概要 再発のリスクの高い皮膚有棘細胞癌患者を対象に、根治的手術と術後の放射線療法を行った後に、抗PD-1抗体のCEMIPLIMABを投与した場合とプラセボとを投与した場合の再発なしで生存する期間などを比較する試験です。 対象となる患者さんは、以下のいずれか1つを満たす必要があります。 初回治療時においては、T4以上の頭頚部発症病変、in transit転移、20㎜以上で節外浸潤のあるリンパ節転移、神経周囲浸潤、初回治療領域における再発例においては、T3以上、N2b以上のリンパ節転移、境界不明な直径20㎜以上の病変。 本試験では実薬であるCEMIPLIMABが入らない(プラセボ)群に割り当てられる場合があります。プラセボ群に割り当てられた患者さんが投与期間中に再発を起こした場合で、患者が希望する場合は、実薬であるCEMIPLIMABの投与を受けられます。 ※注意:治験に参加していただくにあたって、事前に検査を受けていただきます。この検査結果により、参加基準に合わないことが分かった場合は参加できないことがあります。あらかじめご了承ください。その他にも複数の参加基準がありますので、詳しく知りたい方は担当医師にお問い合わせください。
治験担当医師の問い合わせ先
札幌医科大学附属病院 皮膚科 宇原 久
TEL : 011-688-9649
e-mail : uharah@sapmed.ac.jp
② 切除した進行期の黒色腫患者を対象としたアジュバント治療におけるABP 206とオプジーボ® (ニボルマブ) の薬物動態の類似性を評価する試験
試験験の概要 本試験は、登録の12週間以内に手術により腫瘍組織が切除された進行期の黒色腫(皮膚がんの一種)患者を対象とした臨床試験です。本試験は、ABP 206とオプジーボ®の薬物動態(薬剤の投与時点から排泄時点までの経時変化)、ならびに有効性、安全性、免疫原性を検討するものです。対象となる被験者は、ABP 206またはオプジーボ®のいずれかに盲検化された状態で割り付けられます。治療期間は、黒色腫の術後補助療法におけるオプジーボ®の最長投与期間と一致しています。すべての被験者は、疾患の再発、許容できない毒性、または被験者の同意撤回まで、最超1年間の治療を受けます。検査は定期的に実施されます。掲載場所:札幌医科大学医学部皮膚科講座ウェブサイトの「患者さまへ」のページ URL:https://web.sapmed.ac.jp/derm/patients/index.html#tiken
③ 再発若しくは転移性(R/M)又は切除不能な局所進行(LA)の有棘細胞癌患者を有する日本人患者を対象とした、MK-3475Aの安全性及び有効性を評価する第II相試験
治験の概要 再発若しくは転移がある又は根治切除不能な局所進行の有棘細胞癌を有する患者さんを対象として、MK-3475A(ペムブロリズマブとヒアルロニダーゼの配合剤)を皮下投与し、安全性と有効性を調べる試験です。本試験では、参加される患者さん全員にMK-3475Aを投与します。この治験は以下の項目に該当する方を対象としています。1) 有棘細胞癌と診断されている。 2) 再発若しくは転移病変を有する、及び/又は局所病変を有し、手術および放射線療法のいずれによっても治癒できないと診断されている。 前治療に関する主な除外基準はPD-1抗体の投与歴、治験薬投与前4週以内の全身療法歴と2週以内の放射線療法歴です。 募集予定期間:2025年2月7日まで
試験の詳細については下記リンクより確認することができます。jRCTのホームペジhttps://jrct.niph.go.jp/search?page=1にアクセスし、"臨床研究実施計画番号"の欄に"jRCT2041230074"と入力してください。 ※注意:治験に参加していただくにあたって、事前に検査を受けていただきます。この検査結果により、参加基準に合わないことが分かった場合は参加できないことがあります。あらかじめご了承ください。その他にも複数の参加基準がありますので、詳しく知りたい方は担当医師にお問い合わせください。
治験担当医師の問い合わせ先
札幌医科大学附属病院 皮膚科 宇原 久
TEL: 011-688-9649
e-mail: uharah@sapmed.ac.jp
④ 掌蹠膿疱症患者を対象としたKHK4827の第 III 相プラセボ対象二重盲検比較及び非盲検継続投与試験
<募集は終了しました>
治験の概要 掌蹠膿疱症と診断されてから 24 週以上経過し、中等症以上の症状のある18歳以上70歳以下の患者を対象に、KHK4827(ブロダルマブ)の皮下投与とプラセボ(偽薬)を比較して、有効性と安全性を評価する試験です。16 週までは、KHK4827(ブロダルマブ)とプラ セボ(偽薬)のどちらかが投与されますが、16 週経過後はプラセボ(偽薬)群にも KHK4827 (ブロダルマブ)が投与されます。
⑤ がん性皮膚潰瘍を有する患者を対象としたOPF-501Cの臨床試験(探索的試験:第II相)
<募集は終了しました>
試験の概要 がん性皮膚潰瘍がある患者さんのうち、“出血と滲出液の両方がある”方を対象にOPF-501C を1 回または2 回使用したときの出血・滲出液を抑える効果と臭気を和らげる効果(有効性)を探索的に検討すること、及び安全性を確認する試験です。
① 皮膚腫瘍画像データセットの構築と診断支援プログラムの開発
「皮膚腫瘍画像データセットの構築と診断支援プログラムの開発」に関する臨床研究に臨床画像の提供を行っています。提供について札幌医科大学附属病院長の承認を得ています。
倫理審査承認番号: 4549(信州大学医学部医倫理委員会) 研究課題名: 皮膚腫瘍画像データセットの構築と診断支援プログラムの開発 所属(診療科等): 皮膚科 研究責任者(職名): 宇原 久(教授) 研究実施期間: 倫理委員会承認日~2024年3月31日。 研究の意義、目的: 画像解析を用いた新しい皮膚腫瘍の診断方法の確立のため。対象となる患者さん:2005年1月1日から2024年1月31日までに皮膚の拡大写真(ダーモスコピー写真というカメラを皮膚に密着して撮影する特殊な写真)を撮影された方 ※データ収集は後ろ向きで行う。利用する診療記録/検体:診断名、年齢、性別、臨床画像、病変部位、病変サイズ、国籍、メラノーマ既往歴、画像撮影機器、病理検査の有無、再発・転移・外科的処置の有無、ダーモ画像内の病変位置、保険適用の有無(任意)など。他機関への試料・情報の提供方法: 記録媒体の郵送、電子的配信により提供します。研究方法: コンピュータなどを用いて画像解析を行い、新しい皮膚腫瘍の診断法を確立します。研究機関名: 信州大学皮膚科(研究代表者:奥山隆平)問い合わせ先(信州大学): 氏名(所属・役職):皆川茜・助教 電話:0263-37-2647 問い合わせ先(当院): 氏名(所属・職名):佐藤 さゆり・助教電話:011-611-2111 既存の画像や診療記録を研究、調査、集計しますので、新たな診察や検査、検体の採取の必要はありません。利用する情報からは、患者さんを直接特定できる個人情報を削除し、信州大学皮膚科に提供します。研究成果は今後の医学の発展に役立つように学会や学術雑誌などで発表します。また将来的に医療機器等の開発に用いることがあります。また、規制当局等がデータ等を確認させて頂く可能性もあります。しかし、その際も患者様を特定できる個人情報は利用しません。なお、収集する情報の精査過程において、カルテなどの診療情報を信州大学の本研究の担当者が閲覧させていただくことがあります。その場合も、個人情報の取り扱いには十分配慮し、外部に個人情報を持ち出すことはありません。この研究にご自分の診療記録等を利用することをご了解いただけない場合、またご不明な点については、上記問い合わせ先までご連絡くださいますようお願いいたします。画像利用への不参加を申し出られた場合でも、なんら不利益を受けることはありません。ただし、同意取り消しの申し出をいただいたとき、すでに研究成果が論文などで公表されていた場合や、試料や情報が匿名化されて個人が全く特定できない場合などには、結果を廃棄できないこともあり、引き続き使わせていただくことがあります。不同意の場合には、2024年3月1日までに当院問い合わせ先(佐藤さゆり)までご連絡ください。
② 掌蹠末端黒子型黒色腫の外科的深部マージンと予後に関する多機関共同後方視的観察研究
このたび、当院で診察を行った患者さんの診療記録や検査データを用いた以下の研究を実施いたします。本研究は、埼玉医科大学国際医療センター臨床研究IRBの承認を得て、病院長による許可のもと行うものです。本研究では、患者さんに追加でご負担をお願いすることはありませんが、残余検体やカルテ情報等を使用することに賛成でない場合、あるいはご質問がある場合は、患者さんご自身でもその代理人の方でも結構ですので、問い合わせ先までお申し出ください。お申し出いただいても不利益になることは一切ありません。研究の概要について1.研究の対象となる方:2011年 4月 1日~ 2023年 3月31日の期間に 札幌医科大学附属病院 皮膚科 を受診し、掌蹠末端黒子型黒色腫と診断され、手術を実施した患者さんを対象としております。2.研究の目的:遠隔転移のない悪性黒色腫に対して手術(原発腫瘍切除)は現在の第一選択となる治療です。現行の米国や本邦のガイドラインでは腫瘍の厚さに応じて推奨される水平切除マージンが規定されている一方で、深部切除マージンに関しては未だ明確な推奨マージンは言及されていません。腫瘍の厚さと予後は密接な関係があり、完全切除の際には十分な深部切除マージンが必要と一般に考えられていますが、十分な深部切除マージンが本当に予後改善に寄与しているか否かは不明です。日本人に多い掌蹠(手掌・足底)の悪性黒色腫(末端黒子型黒色腫)では深部組織の温存が重要です。他の解剖学的部位とは異なり掌蹠は荷重に耐えうるよう厚い角層や真皮から構成され、脂肪組織はクッションとしても重要な機能を果たします。そのため、過度な深部切除マージンはクッション機能の低下を引き起こし、術後に痛みの発生やたこ・うおのめの発生など患者さんの生活の質(quality of life:QOL)の低下に繋がります。悪性黒色腫の発生が多い欧米では深部切除マージンに関する後方視的観察研究は少数あるものの、掌蹠末端黒子型はほとんど対象に含まれていません。また本邦における掌蹠末端黒子型黒色腫を対象とした深部切除マージンに関する大規模な研究も行われておりません。そのため、本研究では当科を含めた悪性黒色腫の診療に従事する全国の大学病院やがんセンター、主要病院64施設からのデータ提供を得て、深部切除マージンと予後との関係を解析し、適切な深部切除マージンを探索するための有益な情報を得ることを目的とします。深部切除マージン縮小で予後増悪がないことがわかれば本邦の患者さんのQOL向上に繋がります。もし脂肪組織全層を含めた深部マージン切除の方が予後を改善すれば、これまで科学的に不明であった適正な深部切除マージンを解明する一助となります。3.研究期間:病院長の許可後~2026年 6月 14日。研究に用いる試料・情報について1.試料・情報の内容:診療記録、検査データ ※この研究で得られた患者さんの情報は、埼玉医科大学国際医療センター皮膚腫瘍科・皮膚科において、研究責任者である中村泰大が、個人が特定できないように加工した上で管理いたします。そのため、患者さんのプライバシーが侵害される心配はありません。2.試料・情報の取得方法:掌蹠末端黒子型黒色腫と診断され、手術を実施した患者さんの診療記録および検査データ等を用います。3.試料・情報を利用する者(研究実施機関):基盤研究施設および研究者・埼玉医科大学国際医療センター 皮膚腫瘍科・皮膚科 小泉 滋(研究代表者):共同研究施設および研究責任者・旭川医科大学 皮膚科 山本明美(研究責任者)・札幌医科大学 皮膚科 宇原 久(研究責任者)・山形市立病院済生館 皮膚科 角田孝彦(研究責任者)・気仙沼市立病院 皮膚科 芳賀貴裕(研究責任者)・日立総合病院 皮膚科 伊藤周作(研究責任者)・筑波大学 皮膚科 乃村俊史(研究責任者)・自治医科大学 皮膚科 大槻マミ太郎(研究責任者)・群馬大学 皮膚科 安田正人(研究責任者)・君津中央病院 皮膚科 稲福和宏(研究責任者)・千葉大学 皮膚科 猪爪隆史(研究責任者)・順天堂大学浦安病院 皮膚科 金子高英(研究責任者)・埼玉県立がんセンター 皮膚科 石川雅士(研究責任者)・自治医科大学さいたま医療センター 皮膚科 前川武雄(研究責任者)・さいたま赤十字病院 皮膚科 三石 剛(研究責任者)・東京大学医学部 皮膚科 宮川卓也(研究責任者)・帝京大学 皮膚科 多田弥生(研究責任者)・虎の門病院 皮膚科 岸 晶子(研究責任者)・がん研究会有明病院 皮膚腫瘍科 吉野公二(研究責任者)・国立がん研究センター中央病院皮膚腫瘍科 山﨑直也(研究責任者)・慶應義塾大学病院 皮膚科 舩越 建(研究責任者)・都立広尾病院 皮膚科 岩澤うつぎ(研究責任者)・日本医科大学 皮膚科 帆足俊彦(研究責任者)・聖マリアンナ医科大学 皮膚科 門野岳史(研究責任者)・横浜市立大学 形成外科 林 礼人(研究責任者)・信州大学医学部 皮膚科 奥山隆平(研究責任者)・静岡県立静岡がんセンター 皮膚科 清原祥夫(研究責任者)・浜松医科大学 形成外科 中川雅裕(研究責任者)・藤田医科大学皮膚科 有馬 豪(研究責任者)・名古屋大学 皮膚科 横田憲二(研究責任者)・中部国際医療センター 皮膚科 神谷秀喜(研究責任者)・三重大学 皮膚科 北川敬之(研究責任者)・新潟県立がんセンター新潟病院 皮膚科 竹之内辰也(研究責任者)・富山県立中央病院 皮膚科 八田尚人(研究責任者)・福井大学 皮膚科 飯野志郎(研究責任者)・滋賀医科大学 皮膚科 藤本徳毅(研究責任者)・京都府立医科大学 皮膚科 浅井 純(研究責任者)・和歌山県立医科大学 皮膚科 山本有紀(研究責任者)・関西医科大学総合医療センター 皮膚科 清原隆宏(研究責任者)・大阪国際がんセンター 腫瘍皮膚科 大江秀一(研究責任者)・大阪市立総合医療センター 皮膚科 前川直輝(研究責任者)・星ヶ丘医療センター 皮膚科 立花隆夫(研究責任者)・富田林病院 皮膚科 中川浩一(研究責任者)・神戸大学 形成外科 寺師浩人(研究責任者)・神戸市立医療センター中央市民病院 皮膚科 長野 徹(研究責任者)・兵庫医科大学 皮膚科 金澤伸雄(研究責任者)・兵庫県立がんセンター 皮膚科 高井利浩(研究責任者)・市立伊丹病院 皮膚科 南祥一郎(研究責任者)・岡山大学 皮膚科 森実 真(研究責任者)・岡山医療センター 皮膚科 浅越健治(研究責任者)・川崎医科大学 皮膚科 田中 了(研究責任者)・島根大学 皮膚科 山崎 修(研究責任者)・高松赤十字病院 皮膚科 眞鍋恵子(研究責任者)・長崎大学 皮膚科 鍬塚 大(研究責任者)・大分市医師会立アルメイダ病院 形成外科 橋本裕之(研究責任者)・九州大学 皮膚科 伊東孝通(研究責任者)・国立病院機構九州がんセンター 皮膚腫瘍科 内 博史(研究責任者)・久留米大学 皮膚科 名嘉眞武國(研究責任者)・熊本大学病院 皮膚病態治療再建学 福島 聡(研究責任者)・宮崎大学 皮膚科 天野正宏(研究責任者)・国立病院機構鹿児島医療センター 皮膚腫瘍科・皮膚科 松下茂人(研究責任者)4.試料・情報の管理責任者:中村泰大(埼玉医科大学国際医療センター皮膚腫瘍科・皮膚科)。お問合せについて:ご自身の診療記録や検査データを利用されたくない場合、あるいはご質問がある場合には、以下の連絡先までご連絡ください。利用されたくない旨のご連絡をいただいた場合は、研究に用いられることはありません。ただし、ご連絡いただいた時点で、既に研究結果が論文などで公表されていた場合、結果などを廃棄することができないことがありますので、ご了承ください。札幌医科大学附属病院 皮膚科 宇原 久 住所:〒060-8543 札幌市中央区南1条西16丁目291番地 電話:011-611-2111(土日祝日を除く8:30~17:30)
③ 皮膚悪性腫瘍レジストリ研究 Japan Skin Cancer Registry Study (JSCaRS)
研究責任施設である信州大学医学部倫理委員会の承認を受け、研究機関の長の許可を得て実施しています。この研究は、「人を対象とする生命科学・医学系研究に関する倫理指針」の規定により、研究内容の情報を公開することが必要とされています。2024年1月1日
倫理審査承認番号:6025 所属(診療科等):皮膚科 研究責任者(職名):宇原 久 (教授)研究実施期間:倫理委員会承認及び研究機関の長による許可日~2028年11月10日5年ごとに倫理委員会に申請し承認を得た上で上記期間後も研究を継続します。研究の意義、目的:皮膚悪性腫瘍の発生状況,治療,そしてその後の転帰などの情報を多施設共同研究として集積してデータベースを作成することで,本邦における疾患の発生状況や治療の選択,そしてその後の予後についてを明らかにすることが目的となります.また,このようなデータベースが整備されることで新たな治療開発につながる可能性もある,非常に重要な研究となります。対象となる方、症例数:対象となる方:2023年1月1日以降に当院で皮膚悪性腫瘍(メラノーマ,乳房外パジェット病,皮膚リンパ腫,皮膚血管肉腫)にて医療を受けられた方.症例数:30例/年 利用する診療記録:診断名,年齢,性別,身体所見,検査結果,治療の種類,治療の結果,予後など。他機関への情報の提供方法:データベース登録により提供します。研究方法:過去の診療記録より上記の内容を収集し,本邦での発生状況や治療,そして予後について検討します。共同研究機関名:共同研究機関は,日本皮膚悪性腫瘍学会のホームページで公開しています。http://www.skincancer.jp/ 研究代表者:主任施設の名称:信州大学 研究責任者:奥山隆平(信州大学医学部皮膚科・教授)問い合わせ先:氏名(所属・職名): 佐藤さゆり(札幌医科大学皮膚科・助教)電話:011-611-2111 内線:34560既存の診療記録や検査結果を研究、調査、集計しますので、新たな診察や検査、検体の採取の必要はありません。利用する情報からは、患者様を直接特定できる個人情報を削除し、主任施設である信州大学に提供します。研究成果は今後の医学の発展に役立つように学会や学術雑誌などで発表しますが、その際も患者様を特定できる個人情報は利用しません。この研究にご自分の診療記録等を利用することをご了解いただけない場合、またご不明な点については、上記問い合わせ先までご連絡くださいますようお願いいたします。研究不参加を申し出られた場合でも、なんら不利益を受けることはありません。ただし、同意取り消しの申し出をいただいたとき、すでに研究成果が論文などで公表されていた場合や、情報が加工されて個人が全く特定できない場合などには、結果を廃棄できないこともあり、引き続き使わせていただくことがあります。
④ メルケル細胞癌の治療に関する多施設共同後ろ向き観察研究
1.研究の対象 2018年4月1日から2022年3月31日の間に、札幌医科大学附属病院および共同研究機関でメルケル細胞癌に対する手術、放射線治療、薬物療法のいずれかを受けられた方を対象にしています。 2.研究目的・方法 メルケル細胞癌の治療は手術、放射線、薬物療法を組み合わせて行われますが、日本でどのような治療が行われているのか、治療の効果などは、いまだに分かっていません。この研究では、日本国内の施設で治療を受けたメルケル細胞癌患者さんの治療の実態や成績などの情報を集めて比較することで、今後のメルケル細胞癌治療の方針を決める際の有益な情報を得ることを目的としています。 研究の対象となる方の診療録から情報を集め、研究代表施設で集計して解析します。 研究実施期間は研究許可日から2024年3月31日までです。 3.研究に用いる試料・情報の種類 診療録から、生年月日、性別、腫瘍の部位、パフォーマンスステータス、免疫抑制の有無、大きさ、リンパ節転移、遠隔転移、メルケル細胞ポリオーマウイルスの有無、手術日・内容、断端、根治的放射線治療の開始日および線量、術後放射線治療の開始日および照射部位・線量、放射線治療による副作用、再発の有無や状態、薬物療法の有無・開始日、効果・副作用、生存の有無、等の情報を集めます。 4.外部への試料・情報の提供 研究事務局への情報の提供は、セキュリティ対策を行ったパーソナルコンピュータからの電子メールを介してやり取りされます。その際には、パスワードを設定する等のセキュリティ対策を行います。提供される情報は匿名化され、対応表は、各施設の研究責任者が保管・管理します。 5.研究組織・研究責任者 (研究統括者) 国立がん研究センター中央病院皮膚腫瘍科 医長 並川健二郎 (研究代表者・研究事務局) 国立がん研究センター中央病院皮膚腫瘍科 医員 中野英司 (共同研究機関名 / 各機関の研究責任者) 北海道大学 形成外科 前田 拓、旭川医科大学 皮膚科 中川 智絵、 札幌医科大学 皮膚科 宇原 久、 筑波大学 皮膚科 石川 翔一郎、 埼玉県立がんセンター 皮膚科 大芦 孝平、 埼玉医科大学国際医療センター 皮膚腫瘍科・皮膚科 中村 泰大、 がん・感染症センター都立駒込病院 皮膚腫瘍科 西澤 綾 、慶應義塾大学 皮膚科 舩越 建、 東京大学 皮膚科 宮川 卓也、 新潟県立がんセンター新潟病院 皮膚科 竹之内 辰也、 富山県立中央病院 皮膚科 八田 尚人、 信州大学 皮膚科 面高 俊和、 静岡がんセンター 皮膚科 小俣 渡、 名古屋大学 秋山 真志、 名古屋市立大学 中村 元樹、 京都府立医科大学 皮膚科 浅井 純 、大阪国際がんセンター 腫瘍皮膚科 大江 秀一、 愛媛大学 皮膚科 藤澤 康弘、 久留米大学 皮膚科 名嘉眞 健太 、九州大学 皮膚科 伊東 孝通、 熊本大学 皮膚科 福島 聡、 鹿児島医療センター 皮膚腫瘍科・皮膚科 松下 茂人、 北海道大学 皮膚科 柳 輝希 、東北大学 皮膚科 藤村 卓、 自治医科大学 皮膚科 大槻 マミ太郎、 獨協医科大学埼玉医療センター 皮膚科 須山 孝雪、 千葉大学 皮膚科 川島 秀介、 日本医科大学 皮膚科 帆足 俊彦、 横浜市立大学 皮膚科 石川 秀幸、 富山大学 皮膚科 清水 忠道 、岐阜大学 皮膚科 岩田 浩明、 三重大学 皮膚科 北川 敬之、 和歌山県立医科大学 皮膚科 山本 有紀、 神戸大学 皮膚科 藤原 進、 島根大学 皮膚科 山﨑 修 6.お問い合わせ先 本研究に関するご質問等がありましたら下記の連絡先までお問い合わせ下さい。 ご希望があれば、他の研究対象者の個人情報及び知的財産の保護に支障がない範囲内で、研究計画書及び関連資料を閲覧することが出来ますのでお申出下さい。 また、試料・情報が当該研究に用いられることについて患者さんもしくは患者さんの代理人の方にご了承いただけない場合には研究対象としませんので、下記の連絡先までお申出ください。その場合でも患者さんに不利益が生じることはありません。 照会先および研究への利用を拒否する場合の連絡先: 施設研究責任者:札幌医科大学附属病院 皮膚科学講座 教授 宇原久 札幌市中央区南1条西17丁目 平日 TEL 011-611-2111 内線 34550(教室) 夜間休日 TEL 011-611-2111 内線 34620(9階北病棟)
⑤ センチネルリンパ節陽性メラノーマの治療選択と予後に関する多機関共同観察研究について
研究の対象 2018年7月~2021年6月の間に札幌医科大学附属病院皮膚科および共同研究機関にて悪性黒色腫(メラノーマ)に対して原発部位の手術とセンチネルリンパ節生検を受けた方 研究目的・方法 センチネルリンパ節(sentinel node: SN)転移陽性メラノーマ症例に対しての治療実態とその予後を明らかにする目的で行います。メラノーマに対して原発部位の手術とSN生検を受けられ、SN転移があった患者さんのカルテ(診療録)から、情報を抽出し、治療選択により予後が異なるかを検討・評価します。 研究実施期間:病院長承認日~2024年3月31日 予定症例数は当院では5例 研究に用いる試料・情報の種類 カルテから収集される情報には、 SN生検実施日、年齢、性別、発生部位、臨床病型、腫瘍の厚さ、SNの部位、SN転移の有無、SN転移の個数、転移リンパ節の厚み、病期(ステージ)、所属リンパ節郭清術実施の有無、SN転移以外のリンパ節転移の有無とその転移個数、術後補助療法実施したかどうか、術後補助療法に用いた薬剤、最終経過観察日、転移再発の有無、転移再発様式、転移再発までに要した期間、最終転帰、等が含まれます。 外部への情報の提供・情報の保存、管理、二次利用 研究代表施設へのデータの提供は、氏名、カルテ番号等の直ちに個人が判別できる情報が消去された状態で、電子メールを介してやり取りされます。対応表は、各施設の研究責任者が保管・管理します。 〇情報の保存、二次利用 この研究に使用した情報は、研究の中止または研究終了後まで、札幌医科大学皮膚科学講座のパスワード等で管理・制御されたコンピューターに保存します。また、この研究以外の目的で使用されることはありません。 〇情報の管理責任者:この研究で使用する情報は、札幌医科大学附属病院 皮膚科 宇原久が管理します。 上記の事柄についての情報を公開している期間(オプトアウト期間) 2022年10月31日まで 研究組織 研究代表者・研究責任者 国立がん研究センター中央病院 皮膚腫瘍科 山﨑 直也 〒 104-0045 住所 東京都中央区築地5-1-1 電話番号 03-3542-2511 研究事務局 国立がん研究センター中央病院 皮膚腫瘍科 緒方 大 〒 104-0045 住所 東京都中央区築地5-1-1 電話番号 03-3542-2511 お問い合わせ先 本研究に関するご質問等がありましたら下記の連絡先までお問い合わせ下さい。 ご希望があれば、他の研究対象者の個人情報及び知的財産の保護に支障がない範囲内で、研究計画書及び関連資料を閲覧することが出来ますのでお申出下さい。 また、情報が当該研究に用いられることについて患者さんもしくは患者さんの代理人の方にご了承いただけない場合には研究対象としませんので、下記の連絡先までお申出ください。その場合でも患者さんに不利益が生じることはありません。 当院におけるお問い合わせ窓口 〒060-8556 札幌市中央区南1条西17丁目 札幌医科大学附属病院 皮膚科 教授 宇原久 平日 TEL 011-611-2111 内線 34550(教室) 夜間休日 TEL 011-611-2111 内線 34620(9階北病棟看護室)
⑥ 掌蹠膿疱症と喫煙に関する後向き観察研究
研究機関:札幌医科大学医学部皮膚科学講座 研究責任者:札幌医科大学医学部皮膚科学講座 助教 加藤潤史 連絡先:TEL 011-611-2111 内線34550(教室)(平日) TEL 011-611-2111 内線34620(9階北病棟看護室)(夜間休日) 研究期間:病院長承認日~2024年12月31日まで(予定) 1.研究の目的・背景: 掌蹠膿疱症は喫煙歴のある中高年の女性に多いことが知られています。しかしながら喫煙量と皮膚症状の強さにはどのような関係があるのかあきらかにされていません。また受動喫煙の影響についてもわかっていません。そこで掌蹠膿疱症の患者さんの受動喫煙を含む過去の喫煙歴と皮膚症状の強さに関連性があるかどうかを調べることを目的とした研究を行います。解析が進むことで掌蹠膿疱症の患者さんに対して適切な生活指導ができるようになると考えています。 2.研究の方法・対象: 2014年1月1日~2020年3月31日までに札幌医科大学に来院され、掌蹠膿疱症と診断された患者さんの診療録(カルテ)を対象とし、受動喫煙を含む喫煙歴と皮膚症状の強さについて診療録および臨床写真から情報収集を行い、関連性を検討します。そのため、患者さんに負担を要することはありません。情報収集の作業に当たる人員は医師を始めとする医療知識のある研究者です。 3.研究予定期間:病院長承認日~2024年12月31日 4.予定症例数:60症例 5.個人情報保護に関する配慮:閲覧する診療録には個人情報が含まれますが、患者さん個人が特定されない方法で情報を収集します。対象となる患者さんの識別は本研究専用に別途割り振られた研究番号を使用して管理し、個人情報が外に出ることはありません。 6.医学上の貢献:この研究の成果は、学会発表や医学雑誌で公表され、医学の発展に寄与します。 7.研究対象者等及びその関係者からの相談等への対応に関する情報: 本研究の対象になられる方で、ご自身のデータの利用を除外してほしいと希望される方は、上記連絡先まで2021年12月31日までに申し出てください。あなたに関わる研究結果は破棄され、診療記録なども、それ以降は研究目的に用いられることはありません。 ただし、ご連絡をいただいた時点で既に研究結果が論文などに公表されている場合や、研究データの解析が終了している場合には、解析結果等からあなたに関するデータを取り除くことが出来ず、研究参加を取りやめることが出来なくなります。 除外のお申し出により不利益を被ることは一切ありません。
⑦ 皮膚腫瘍の診断と治療効果の評価および経過観察のためのバイオマーカーの探索(前向き観察研究)
がんの分子標的治療、免疫チェックポイント阻害療法を行う上で、そのがんがもつ遺伝子異常を知ることは重要です。しかし、日本人の皮膚悪性腫瘍の遺伝子異常については、網羅的な解析研究が行われていません。本研究では日本人の皮膚がんの遺伝子情報及び臨床情報を集め、あらたな診断、治療のバイオマーカーを探索します。また、国内のがんゲノム情報のデータベースである国立がん研究センターがんゲノム情報管理センター(C-CAT)の集積情報とデータを比較することで、日本人の皮膚悪性腫瘍の遺伝子異常の全体像を明らかにします。【連絡先】 肥田時征 〒060-8543 札幌市中央区南1条西16丁目 札幌医科大学皮膚科 平日 TEL 011-611-2111 内線34550 (皮膚科教室)夜間休日 TEL 011-611-2111 内線 34620 (9階北病棟看護室)
⑧ 皮膚腫瘍画像データセットの構築と診断支援プログラムの開発
札幌医科大学附属病院 皮膚科に通院中または過去に通院・入院された患者さんまたはご家族の方へ: 当科における画像提供にご協力をお願いいたします。 2020年5月1日 信州大学で実施されている「皮膚腫瘍画像データセットの構築と診断支援プログラムの開発」に関する臨床研究に臨床画像の提供を行っています。提供について、札幌医科大学附属病院長の承認を得ています。研究課題名:皮膚腫瘍画像データセットの構築と診断支援プログラムの開発 所属(診療科等):皮膚科 当院担当者(職名):宇原 久(教授) 研究実施期間:倫理委員会承認日~2024年10月31日 研究の意義、目的:画像解析を用いた新しい皮膚腫瘍の診断方法の確立のため 対象となる患者さん:2005年1月1日から2021年3月31日までに皮膚の拡大写真(ダーモスコピー写真というカメラを皮膚に密着して撮影する特殊な写真)を撮影された方 利用する診療記録/検体:診断名、年齢、性別、臨床画像、病変部位、病変サイズ、など 他機関への試料・情報の提供方法:記録媒体の郵送、電子的配信により提供します 研究方法:コンピュータなどを用いて画像解析を行い、新しい皮膚腫瘍の診断法を確立します。 研究機関名:信州大学皮膚科(研究代表者:奥山隆平) 問い合わせ先(信州大学):氏名(所属・役職):皆川茜・助教 電話:0263-37-2647 問い合わせ先(当院):氏名(所属・役職):神谷崇文・講師 電話:011-688-9649 内線:34550 既存の画像や診療記録を研究、調査、集計しますので、新たな診察や検査、検体の採取の必要はありません。 利用する情報からは、患者さんを直接特定できる個人情報を削除し、信州大学皮膚科に提供します。研究成果は今後の医学の発展に役立つように学会や学術雑誌などで発表します。また将来的に医療機器等の開発に用いることがあります。また、規制当局等がデータ等を確認させて頂く可能性もあります。しかし、その際も患者様を特定できる個人情報は利用しません。 なお、収集する情報の精査過程において、カルテなどの診療情報を信州大学の本研究の担当者が閲覧させていただくことがあります。その場合も、個人情報の取り扱いには十分配慮し、外部に個人情報を持ち出すことはありません。 この研究にご自分の診療記録等を利用することをご了解いただけない場合、またご不明な点については、上記問い合わせ先までご連絡くださいますようお願いいたします。 画像利用への不参加を申し出られた場合でも、なんら不利益を受けることはありません。ただし、同意取り消しの申し出をいただいたとき、すでに研究成果が論文などで公表されていた場合や、試料や情報が匿名化されて個人が全く特定できない場合などには、結果を廃棄できないこともあり、引き続き使わせていただくことがあります。不同意の場合には、2020年10月31日までに当院問い合わせ先(神谷崇文)までご連絡ください。
⑨ コリン性蕁麻疹における発汗指導の有効性に関する後向き観察研究
研究課題:コリン性蕁麻疹における発汗指導の有効性に関する後向き観察研究 研究機関:札幌医科大学医学部皮膚科学講座
研究責任者:札幌医科大学医学部皮膚科学講座 助教 菅裕司 連絡先:TEL 011-611-2111 内線34550(教室)(平日)
TEL 011-611-2111 内線34620(9階北病棟看護室)(夜間休日) 研究期間:病院長承認日~2024年12月31日まで(予定) 1.研究の目的・背景: コリン性蕁麻疹は運動や入浴などの体温上昇によって生じる刺激誘発型蕁麻疹です。刺激誘発型蕁麻疹では、誘発する刺激の同定とその除去が病勢コントロールに推奨されているものの、入浴や発汗を日常から避けることは困難です。一方で、発汗障害を伴うコリン性蕁麻疹においては、積極的な発汗がむしろ症状改善に有効であった少数の症例報告が存在するものの科学的根拠に乏しいのが現状です。そこで、コリン性蕁麻疹における発汗指導の有効性について検討します。解析が進むことで、治療選択肢が広がり治療方針に影響を与えるのではないかと考えています。 2.研究の方法・対象: 2013年10月1日から2019年4月30日の期間に、札幌医科大学皮膚科においてコリン性蕁麻疹の診断を受け治療をうけられた方々の診療録(カルテ)を対象とし、発汗障害の有無、発汗指導の有無とその治療反応について診療録から情報収集を行い、治療効果について比較し検討します。そのため、患者さんに負担を要することはありません。情報収集の作業に当たる人員は医師を始めとする医療知識のある研究者です。 3.研究予定期間:病院長承認日~2024年12月31日 4.予定症例数:50症例 5.個人情報保護に関する配慮:閲覧する診療録には個人情報が含まれますが、患者さん個人が特定されない方法で情報を収集します。対象となる患者さんの識別は本研究専用に別途割り振られた研究番号を使用して管理し、個人情報が外に出ることはありません。 6.医学上の貢献:この研究の成果は、学会発表や医学雑誌で公表され、医学の発展に寄与します。 7.研究対象者等及びその関係者からの相談等への対応に関する情報: 本研究の対象になられる方で、ご自身のデータの利用を除外してほしいと希望される方は、上記連絡先まで2020年12月31日までに申して出てください。あなたに関わる研究結果は破棄され、診療記録なども、それ以降は研究目的に用いられることはありません。 ただし、ご連絡をいただいた時点で既に研究結果が論文などに公表されている場合や、研究データの解析が修了している場合には、解析結果等からあなたに関するデータを取り除くことが出来ず、研究参加を取りやめることが出来なくなります。 除外のお申し出により不利益を被ることは一切ありません。
⑩ 2014年8月1日から2024年8月1日の間に札幌医科大学附属病院皮膚科において薬疹、紅皮症、じんましん、乾癬、アトピー性皮膚炎などの皮膚が赤く、かゆくなる皮膚疾患で治療を受けられた方へ
研究課題名:「炎症性皮膚疾患において免疫担当細胞と組織中サイトカインが
病理組織構築に与える影響についての後方視的研究」へご協力のお願い 研究機関名 札幌医科大学附属病院
研究機関長 病院長 渡辺 敦
研究責任者 札幌医科大学附属病院 皮膚科 准教授 肥田 時征
研究分担者 札幌医科大学附属病院 皮膚科 助教 菅 裕司
札幌医科大学附属病院 皮膚科 助教 神谷 詩織
札幌医科大学附属病院 皮膚科 助教 加藤 潤史
札幌医科大学附属病院 皮膚科 助教 堀本 浩平
札幌医科大学附属病院 皮膚科 助教 佐藤 さゆり
札幌医科大学附属病院 皮膚科 教授 宇原 久
1.研究の概要 ○研究の目的: 乾癬、アトピー性皮膚炎、薬疹、じんましん、紅皮症などの皮膚が赤くかゆくなる疾患(炎症性皮膚疾患)の症状は、その程度によってさまざまです。正しい診断のために皮膚の一部を取る(皮膚生検と病理組織検査といいます)ことがあります。しかし、大学病院を受診する患者さんは、経過が長く、典型的な病理組織が確認できず診断が難しくなることがあります。
本研究では、札幌医科大学附属病院皮膚科で炎症性皮膚疾患の診断を受けた方で、病理組織像をさらに詳しく調べたり、治療によって起きた病理組織像の変化を教科書的な病理組織像と比較することで、炎症性皮膚疾患の診断精度の向上に役立てるのが目的です。
2) 研究の意義・医学上の貢献
この研究で得られた成果は、札幌医科大学附属病院の患者さんに限らず、広く全国の同じ疾患の患者さんの診断精度の向上に貢献できる可能性があります。また、病理組織を詳細に検討することで新しい治療の開発につながるような知見が得られるかもしれません。
2.研究の方法 ○研究対象者: 2014年8月1日から2024年8月1日の間に札幌医科大学附属病院において、皮膚生検をうけて炎症性皮膚疾患と診断された方や、すでに炎症性皮膚疾患と診断されて治療経過中に皮膚生検をうけた方が研究対象者です。 ○研究期間: 病院長承認後~2026年3月31日 ○予定症例数: 200例を予定しています。 ○研究方法: 2014年8月1日から2024年8月1日の間に札幌医科大学附属病院において、皮膚生検をうけて炎症性皮膚疾患と診断された方や、すでに炎症性皮膚疾患と診断されて治療経過中に皮膚生検をうけた方で、過去に採取した組織と治療内容との関連性を解析します。そのために、病理組織所見を詳細に検討して免疫染色を行います。 ○使用する試料: 2014年8月1日から2024年8月1日の間に札幌医科大学附属病院において、皮膚生検をうけて炎症性皮膚疾患と診断された方や、すでに炎症性皮膚疾患と診断されて治療経過中に皮膚生検をうけた方の病理組織を使用します。 ○使用する情報: 大学病院のカルテに記載してある情報の中から以下の項目を抽出して使用させていただきます。分析する際には氏名、生年月日などのあなたを特定できる情報は削除して使用します。また、あなたの情報などが漏洩しないようプライバシーの保護には細心の注意をはらいます。
・年齢、性別、身長、体重、診断名、既往歴、家族歴
・皮膚症状の状態、全身状態
・血液検査結果
・以前に受けた治療内容 試料・情報の利用開始予定日
試料・情報の利用を開始する予定日は、2024年12月16日です。
3.試料・情報の保存、二次利用: この研究に使用した試料・情報は、研究終了後、研究完了(中止)報告書を提出した日から5年が経過した日までの間、札幌医科大学附属病院皮膚科で保存させていただきます。電子情報の場合はパスワード等で管理・制御されたコンピュータに保存します。その他の試料・情報は施錠可能な保管庫に保存します。
なお、保存された試料・情報を用いて新たな研究を行う際は、臨床研究審査委員会(倫理審査委員会)で承認を得ます。
試料・情報の管理について責任を有する者の氏名又は名称
札幌医科大学附属病院 病院長 渡辺 敦
4. 研究結果の公表:
この研究の結果は学会や論文で発表します。その際も氏名、生年月日などのあなたを特定できるデータは一切含まないようにします。
この研究にご質問等がありましたら下記の連絡先までお問い合わせ下さい。また、あなたの試料・情報が研究に使用されることについて、あなたもしくは代理人の方にご了承いただけない場合には研究に使用しませんので、2024年11月30日までの間に下記の連絡先までお申し出ください。お申し出をいただいた時点で、研究に用いないように手続きをして、研究に用いられることはありません。この場合も、その後の診療など病院サービスにおいて患者さんに不利益が生じることはありません。
ご連絡いただいた時点が上記お問い合わせ期間を過ぎていて、あなたを特定できる情報がすでに削除されて研究が実施されている場合や、個人が特定できない形ですでに研究結果が学術論文などに公表されている場合は、解析結果からあなたに関する情報を取り除くことができないので、その点はご了承ください。
<問い合わせ・連絡先>
札幌医科大学附属病院 皮膚科
氏名:肥田 時征
電話:011-611-2111 内線 34550(教室) 平日:8時45分~17時30分
011-611-2111 内線 34620(7階南病棟看護室) 夜間、休日、時間外
⑪ 皮膚がんにおける免疫染色と治療効果・進行度の関連についての後方視的研究
○研究の背景・目的: 近年、転移をした悪性黒色腫では免疫チェックポイント阻害薬(免疫を高める点滴)や分子標的薬(がんの目印をピンポイントで攻撃する飲み薬)などの新しい治療法も出てきています。この様な新しい治療法が効きやすい患者さんと効きにくい患者さんでIDO-1(アイディーオーワン)という酵素やPD-1(ピーディーワン)やPD-L1(ピーディーエルワン)という蛋白の発現に差があるのではないかといわれてきています。また、悪性黒色腫以外の皮膚がんについてほとんど解明されていません。私たちは、悪性黒色腫を含む皮膚がんにおいてこれらの解明がすすめば、患者さんの経過観察や進行した患者さんの治療方針の決定にも役立つのではないかと考えています。○方法・研究対象・利用する情報: 2010年1月1日から2021年9月30日の間に札幌医大皮膚科において皮膚がんと診断されて治療をうけられた方々の診療録(カルテ)を対象とし、治療内容、転移の有無、治療効果についての情報収集を試みます。また、過去に行った細胞検査または手術時の腫瘍組織を用いてPD-1/PD-L1(ピーディーワン/ピーディーエルワン)などの免疫染色を行います。また、皮膚の良性疾患との比較検討のため、色素性母斑(ほくろ)と診断されて治療を受けられた方々の手術時の組織を用いて免疫染色を行います。情報収集の作業に当たる人員は医師をはじめとする医療知識のある研究者です。この作業で収集した情報を通じて、染色(細胞のマーカーに色を付けて判定しやすくすること)の程度で、皮膚がんの進行度、治療効果が異なるかどうかについて検証します。〇研究期間: 病院承認日~2023年12月31日 〇予定症例数: 70症例 ○個人情報保護に関する配慮: 閲覧する診療録には個人情報が含まれますが、患者さん個人が特定されない方法で情報を収集します。対象となる患者さんの識別は本研究専用に別途割り振られた研究番号を使用して管理し、個人情報が外に出ることはありません。〇医学上の貢献: この研究の成果は, 学会発表や医学雑誌で公表され、医学の発展に寄与されます。〇研究に診療データを提供したくない場合の措置: 患者さからのご希望があれば、その方の診療録は研究に利用しないようにしますので、次の連絡先まで申して出てください。上記の事柄についての情報を公開している期間(オプトアウト期間):2022年9月30日まで。 照会先: 〒060-8556 札幌市中央区南1条西17丁目 札幌医科大学 皮膚科 加藤潤史 平日 TEL 011-611-2111 内線 34550(教室) 夜間休日 TEL 011-611-2111 内線 34620(9階北病棟看護室)
⑫ 皮膚悪性黒色腫の臨床統計調査について
1. 研究の目的:皮膚悪性黒色腫は欧米に比べて本邦での発生数は少なく,単一施設での症例集積が困難な悪性腫瘍の一つです。従って、多施設の症例を集積してその発生状況の傾向や、現在行われている検査や治療の妥当性について検討する必要がある。皮膚悪性黒色腫の症例数、新規発症数、発症年齢など基本的臨床統計の把握し、累積データから、病型の変動、検査法の使用頻度や精度の推定、治療成績の推移、生存率などの予後調査を行うことが目的です。 2. 研究対象者: 2006年1月1日から2025年12月31日までに当院で悪性黒色腫と診断された患者さん 研究期間:病院長承認後~2026年12月31日 。3. 研究の方法:登録専用ホームページ(大学病院医療情報ネットワーク研究センターのシステム)に匿名化した、年齢、性別、腫瘍の状態、予後、治療の項目を入力します。4. 試料・情報の項目:診療記録(年齢,性別,腫瘍の状態,治療経過,予後など)5. 情報の管理は筑波大学で行われる。6. 研究機関名および研究責任者名:共同研究施設:27施設 (下記に記載しています) 7. 収集したデータは統計学的な処理をし、予後因子等について検討を行います。本邦でも診療ガイドラインが作成されていますが、新たなEBM、重要なデータを収集することによりガイドラインの改訂にも役立ちます。 8. 本研究への参加を希望されない場合: 患者さんやご家族が本研究への参加を希望されず、情報の利用又は提供の停止を希望される場合は、下記の問い合わせ先へご連絡ください。すでに研究結果が公表されている場合など、ご希望に添えない場合もございます。 照会先:〒060-8556 札幌市中央区南1条西17丁目 宇原 久(札幌医科大学医学部皮膚科 教授) 肥田 時征(同 講師)加藤潤史(同 助教)平日 TEL 011-611-2111 内線 34550(教室) 夜間休日 TEL 011-611-2111 内線 34620(9階北病棟看護室) 参加施設:筑波大学 皮膚科、札幌医科大学 皮膚科、旭川医科大学 皮膚科、北海道大学 形成外科、東北大学 皮膚科、埼玉県立がんセンター 皮膚科、埼玉医科大学 皮膚科、埼玉医科大学国際医療センター 皮膚腫瘍科、東京大学 皮膚科、日本医科大学 皮膚科、国立がんセンター中央病院 皮膚科、信州大学 皮膚科、新潟県立がんセンター 皮膚科、富山県立中央病院 皮膚科、浜松医科大学 皮膚科、県立静岡がんセンター 皮膚科、岐阜大学 皮膚科、名古屋大学 皮膚科、大阪市立大学 皮膚科、京都府立医科大学 皮膚科、神戸大学 皮膚科、産業医科大学 皮膚科、九州大学 皮膚科、福岡大学 皮膚科、熊本大学 皮膚科、岡山大学皮膚科、 鹿児島大学 皮膚科。
⑬ メルケル細胞がんにおける免疫チェックポイント阻害薬治療の効果予測に関する研究
○研究の背景・目的: メルケル細胞がんの治療としてのバベンチオという薬剤が使用されていますが、治療効果を予測、評価する有用なバイオマーカーはまだに見つかっていません。これまでの研究で、糖代謝経路に関わる酵素の一つであるグルコースー6-リン酸脱水素酵素の発現や活性が、腫瘍の免疫活性の強さを調べるマーカーとして有用であることわかってきました。そこで、全国13施設において免疫チェックポイント阻害薬(バベンチオ®)で治療したメルケル細胞がんの患者さんを対象に、手術で採取した組織を用いて計測したグルコースー6-リン酸脱水素酵素の発現、活性が免疫チェックポイント阻害薬の治療効果予測・判定に有用であるかどうかを解析するのが目的です。 ○方法・研究対象・利用する情報・試料:2015年1月1日から病院長承認日の期間にメルケル細胞がんに対してバベンチオによる治療を受けた患者さんが対象です。検査や手術などで採取されたメルケル細胞がんの組織を用いて、グルコースー6-リン酸脱水素酵素の発現と活性を調べます。また、診療録(カルテ)を対象とし、年齢、性別、腫瘍の大きさ、基礎疾患、治療内容、再発の有無などについての情報収集を行います。情報収集の作業に当たる人員は医師をはじめとする医療知識のある研究者です。〇研究期間: 病院長承認日から2026年3月31日 〇予定症例:全国13施設の病院において約50名の方に参加していただく予定です。(当院参加予定は4名です) 〇患者さんへの不利益について: 当研究は過去に採取した組織の一部を使用と診療録(カルテ)からの情報収集のため、患者さんに生じる負担、リスクはありません。またこの研究の参加による直接的な利益もありません。 ○個人情報保護に関する配慮: 閲覧する診療録には個人情報が含まれますが、患者さん個人が特定されない方法で情報を収集します。対象となる患者さんの識別は本研究専用に別途割り振られた研究番号を使用して管理し、個人情報が外に出ることはありません。また、この研究以外の目的で使用されることはありません。 〇外部への試料・情報の提供: この研究に使用する試料と情報は、以下の共同研究機関に提供させていただきます。提供の際、氏名、生年月日などのあなたを特定できる情報は削除し、提供します。 提供先:名古屋市立大学病院 加齢・環境皮膚科学 中村元樹 〇この研究で使用する試料・情報は、以下の責任者が管理します。 札幌医科大学附属病院 皮膚科 加藤潤史 〇試料・情報の保存、二次利用: この研究に使用した情報は、研究の中止または研究終了後5年間、札幌医科大学皮膚科学講座のパスワード等で管理・制御されたコンピューターに保存します。また、この研究以外の目的で使用されることはありません。 〇医学上の貢献: この研究の成果は, 学会発表や医学雑誌で公表され、医学の発展に寄与されます。 〇研究に診療データを提供したくない場合の措置: 患者さんからのご希望があれば、その方の診療録は研究に利用しないようにしますので、2021年8月31日までの間に下記の連絡先まで申し出てください。お申し出をいただいた時点で、研究に用いないように手続をして、研究に用いられることはありません。この場合も、その後の診療など病院サービスにおいて患者の皆様に不利益が生じることはありません。ただし、御連絡をいただいた時点で既に研究結果が論文などに公表されている場合や、研究データの解析が終了している場合には、解析結果等からあなたに関するデータを取り除くことができず、研究参加を取りやめることができなくなります。 〇上記の事柄についての情報を公開している期間(オプトアウト期間): 2021年8月31日まで 〇研究組織 <研究代表者> 名古屋市立大学病院 加齢・環境皮膚科学 中村元樹 名古屋市瑞穂区瑞穂町字川澄1 <共同参加施設(50音順)および各施設研究責任者> 大阪市立大学大学院医学研究科 皮膚病態学 小澤俊幸; 金沢大学医薬保険研究域医学系 皮膚分子病態学 小林忠弘; 熊本大学大学院生命科学研究部 皮膚病態治療再建学講座 福島聡 ;群馬大学大学院医学系研究科 皮膚科学 安田正人; 国立がん研究センター中央病院 皮膚腫瘍科 緒方大; 埼玉医科大学国際医療センター 皮膚腫瘍科・皮膚科 中村泰大; 佐賀大学医学部内科学 皮膚科 永瀬浩太郎; 札幌医科大学 皮膚科 加藤潤史; 静岡がんセンター 皮膚科 吉川周佐; 信州大学 皮膚科 木庭幸子; 自治医科大学 皮膚科 前川武雄; 横浜市立大学大学院医学研究科 環境免疫病態皮膚科学 石川秀幸。当院におけるお問い合わせ窓口: 〒060-8556 札幌市中央区南1条西17丁目 札幌医科大学 皮膚科 加藤潤史 平日 TEL 011-611-2111 内線 34550(教室) 夜間休日 TEL 011-611-2111 内線 34620(9階北病棟看護室)
⑭ 悪性汗器官腫瘍に対する化学療法の有効性に関する後方視的検討
○研究の背景・目的: この説明文書は, 汗孔がん、汗腺がんなどの悪性汗器官腫瘍(あくせいかんきかんしゅよう)に対する化学療法の臨床効果と有害事象の相関を評価・解析に関する研究(研究課題名:悪性汗器官腫瘍に対する化学療法の有効性に関する後方視的検討)について説明したものです。 悪性汗器官腫瘍は皮膚がんの中でも稀な腫瘍であり、多くの場合は外科的切除により根治が可能ですが、リンパ節転移や遠隔転移をきたした場合、その希少性から有効性の高い薬剤の開発は進んでおらず、また、確立された治療方法もほとんどない状況です。単一施設の解析では、患者さんの人数も少ないため、本研究では、群馬大学医学部附属病院皮膚科を中心として、全国30施設と共同で研究を行うことにより、悪性汗器官腫瘍に対して、化学療法を受けた方に対して、臨床効果と有害事象の解析を行い評価することを目的としています。 ○方法・研究対象・利用する情報: 2010年1月1日から2020年12月31日までに悪性汗器官腫瘍の診断で化学療法を受けられた方を対象に致します。診療録(カルテ)から、年齢、性別、原発巣部位、原発巣サイズ、病歴に関する情報(前治療歴、後治療歴)、臨床病期、転移部位、血液所見、病理学的所見(病型)、治療(投与薬剤、期間、中断、放射線療法)、治療反応性・予後、副作用などの情報収集を行います。情報収集の作業に当たる人員は医師をはじめとする医療知識のある研究者です。〇研究期間: 病院長承認日から2025年3月31日 〇予定症例:全国30施設の病院において約150名の方に参加していただく予定です。 (当院参加予定は5名です) 〇患者さんへの不利益について: 当研究は過去の診療録(カルテ)からの情報収集のため、患者さんに生じる負担、リスクはありません。またこの研究の参加による直接的な利益もありません。 〇外部への情報の提供: この研究に使用する情報は、以下の共同研究機関に提供させていただきます。提供の際、氏名、生年月日などのあなたを特定できる情報は削除し、提供します。 提供先:群馬大学医学部附属病院 皮膚科 講師 安田正人 〇情報の保存、二次利用: この研究に使用した情報は、研究の中止または研究終了後5年間まで、札幌医科大学皮膚科学講座のパスワード等で管理・制御されたコンピューターに保存します。また、この研究以外の目的で使用されることはありません。 ○個人情報保護に関する配慮: 閲覧する診療録には個人情報が含まれますが、患者さん個人が特定されない方法で情報を収集します。対象となる患者さんの識別は本研究専用に別途割り振られた研究番号を使用して管理し、個人情報が外に出ることはありません。 〇情報の管理責任者: この研究で使用する情報は、以下の責任者が管理します。 札幌医科大学附属病院 皮膚科 加藤潤史 〇医学上の貢献: この研究の成果は, 学会発表や医学雑誌で公表され、医学の発展に寄与されます。 〇研究に診療データを提供したくない場合の措置: 患者さんからのご希望があれば、その方の診療録は研究に利用しないようにしますので、次の連絡先まで申し出てください。お申し出をいただいた時点で、研究に用いないように手続をして、研究に用いられることはありません。この場合も、その後の診療など病院サービスにおいて患者の皆様に不利益が生じることはありません。ただし、御連絡をいただいた時点で既に研究結果が論文などに公表されている場合や、研究データの解析が終了している場合には、解析結果等からあなたに関するデータを取り除くことができず、研究参加を取りやめることができなくなります。 〇上記の事柄についての情報を公開している期間(オプトアウト期間):2021年8月31日まで 〇研究組織 <研究代表者> 研究代表者(研究全体の責任者): 群馬大学医学部附属病院 皮膚科 講師 安田正人 電話番号 027-220-7111 (内線 8284) <共同参加施設> 札幌医科大学皮膚科、国立がん研究センター中央病院皮膚腫瘍科、東京都立駒込病院皮膚腫瘍科、岩手医科大学皮膚科、山形大学皮膚科、新潟県立がんセンター新潟病院皮膚科、筑波大学皮膚科、福井大学皮膚科、自治医科大学皮膚科、埼玉医科大学国際医療センター腫瘍皮膚科、埼玉県立がんセンター皮膚科、慶應義塾大学皮膚科、千葉大学皮膚科、静岡県立静岡がんセンター皮膚科、信州大学皮膚科、三重大学皮膚科、名古屋市立大学皮膚科、滋賀医科大学皮膚科、京都大学皮膚科、京都府立医科大学皮膚科、和歌山医科大学皮膚科、大阪国際がんセンター腫瘍皮膚科、兵庫県立がんセンター皮膚科、川崎医科大学皮膚科、産業医科大学皮膚科、久留米大学皮膚科、長崎大学皮膚科、佐賀大学皮膚科、熊本大学皮膚科、琉球大学皮膚科 。当院におけるお問い合わせ窓口 〒060-8556 札幌市中央区南1条西17丁目 札幌医科大学 皮膚科 加藤潤史 平日 TEL 011-611-2111 内線 34550(教室) 夜間休日 TEL 011-611-2111 内線 34620(9階北病棟看護室)
⑮ 皮膚悪性腫瘍の受診動機と病期・予後に関する多施設共同観察研究
○研究の背景・目的: 皮膚がん発生数は世界的に増加傾向にあり、欧米では本邦に比べて皮膚がんに対する社会的関心が高いとされており、欧米では受診動機と予後の関連についての報告が複数なされている一方で、本邦では罹患率の低さから詳細な調査報告はほとんど存在しません。一方で、皮膚がん、特に悪性黒色腫においては、本邦の症例は診断時に進行期である割合が欧米に比べて高いことが報告されています。皮膚がんは早期から肉眼的に視認可能であるため、有効な啓発活動が早期受診に結び付く可能性があると考え、その有効な啓発活動の具体策を検討したいと考えています。そのため、本研究では我が国における皮膚がんの罹患数を把握し、皮膚がん患者さんの受診動機と病期・予後に関して調査を行い、早期受診を促すための方策を提言することを目的としています。 ○方法・研究対象・利用する情報: 2019年4月1日から2021年11月30日までに皮膚がんを主訴に受診された方を対象に行 います。カルテから、年齢、性別、紹介経路、部位、診断名、病期、腫瘍に気付いてから最初に医療機関を受診するまでの期間、主訴、受診動機、受診理由、生活歴、家族歴、 皮膚がんの認識有り無しなどの項目情報を抽出し、調査を行います。情報収集の作業に当 たる人員は医師をはじめとする医療知識のある研究者です。 〇研究期間: 病院長承認日から2025年3月31日 〇予定症例: この研究には、全国の協力施設の病院において約5000名の方に参加していただく予定です。(当院参加予定は150名です。) 〇患者さんへの不利益について: 当研究は診療録(カルテ)からの情報収集のため、患者さんに生じる負担、リスクはありません。またこの研究の参加による直接的な利益もありません。 ○個人情報保護に関する配慮: 閲覧する診療録には個人情報が含まれますが、患者さん個人が特定されない方法で情報を収集します。対象となる患者さんの識別は本研究専用に別途割り振られた研究番号を使用して管理し、個人情報が外に出ることはありません。また、この研究以外の目的で使用されることはありません。 〇外部への情報の提供: この研究に使用する情報は、以下の共同研究機関に提供させていただきます。提供の際、氏名、生年月日などのあなたを特定できる情報は削除し、提供します。 提供先:国立がん研究センター中央病院 皮膚腫瘍科 緒方 大 〇この研究で使用する情報は、以下の責任者が管理します。 札幌医科大学附属病院 皮膚科 加藤潤史 〇情報の保存、二次利用: この研究に使用した情報は、研究の中止または研究終了後5年間、札幌医科大学皮膚科学講座のパスワード等で管理・制御されたコンピューターに保存します。また、この研究以外の目的で使用されることはありません。 〇医学上の貢献: この研究の成果は、学会発表や医学雑誌で公表され、医学の発展に寄与されます。 〇研究に診療データを提供したくない場合の措置: 患者さんからのご希望があれば、その方の診療録は研究に利用しないようにしますので、2021年11月30日までの間に下記の連絡先まで申し出てください。お申し出をいただいた時点で、研究に用いないように手続をして、研究に用いられることはありません。この場合も、その後の診療など病院サービスにおいて患者の皆様に不利益が生じることはありません。ただし、御連絡をいただいた時点で既に研究結果が論文などに公表されている場合や、研究データの解析が終了している場合には、解析結果等からあなたに関するデータを取り除くことができず、研究参加を取りやめることができなくなります。 〇上記の事柄についての情報を公開している期間(オプトアウト期間): 2021年11月30日まで 〇研究組織 <研究代表者> 国立がん研究センター中央病院 皮膚腫瘍科 緒方 大 東京都中央区築地5-1-1 電話番号 03-3542-2511<共同参加施設および各施設研究責任者> 新潟県立新潟がんセンター 竹之内辰也、 慶応大学皮膚科 中村善雄、 鳥取大学皮膚科 後藤寛之、 信州大学皮膚科 面高俊和、札幌医科大学附属病院 皮膚科 加藤潤史、宮崎大学皮膚科 持田耕介、名古屋市立大学皮膚科 中村元樹、佐賀大学皮膚科 永瀬浩太郎 〇当院におけるお問い合わせ窓口:〒060-8556 札幌市中央区南1条西17丁目 札幌医科大学附属病院 皮膚科 助教 加藤潤史 平日 TEL 011-611-2111 内線 34550 (教室) 夜間休日 TEL 011-611-2111 内線 34620 (9階北病棟看護室)
⑯ BRAF陽性悪性黒色腫に対するBRAF・MEK阻害薬および免疫チェックポイント阻害薬の臨床効果に関する多機関共同後ろ向き観察研究
1.研究の対象 2016年4月1日から2021年3月31日までに、BRAF(ビーラフ)遺伝子変異を有する悪性黒色腫(メラノーマ)に対して、ダブラフェニブ(商品名:タフィンラー)・トラメチニブ(商品名:メキニスト)併用療法、エンコラフェニブ(商品名:ビラフトビ)・ビニメチニブ(商品名:メクトビ)併用療法、ニボルマブ(商品名:オプジーボ)やペムブロリズマブ(商品名:キイトルーダ)の単独療法、ニボルマブとイピリムマブ(商品名:ヤーボイ)の併用療法のうち、いずれか1つ以上のがん薬物療法を受けた20歳以上の方を対象にしています。 なお、手術後に再発予防目的(術後補助療法といいます)で上記の薬剤を投与された方は、本研究の対象ではありません。 2.研究目的・方法 BRAF遺伝子変異を有する悪性黒色腫(BRAF陽性悪性黒色腫)に対するがん薬物療法は、ダブラフェニブ・トラメチニブ併用療法やエンコラフェニブ・ビニメチニブ併用療法などのBRAF・MEK阻害薬と、ニボルマブやペムブロリズマブの単独療法、ニボルマブとイピリムマブの併用療法といった免疫チェックポイント阻害薬の2種類に大別されます。しかしながら、そのどちらを先に投与した方がより有効なのか、いまだに分かっていません。海外では主に白人を対象とした臨床試験が進行中ですが、日本からはそれらの臨床試験に参加しておらず、日本人の治療成績に関する情報は十分ではありません。 この研究では、日本国内の施設で治療を受けたBRAF陽性悪性黒色腫患者さんの治療成績をはじめとした臨床情報を集めて比較することで、今後のBRAF陽性悪性黒色腫の治療方針を決める際の有益な情報を得ることを目的としています。診療録から臨床情報を抽出し、研究代表施設で集計します。 研究実施期間は研究許可日から2023年11月30日までです。 予定症例数は当院で8例程度、本研究全体で400例程度です。 3.研究に用いる情報の種類 診療録から収集される情報には、生年月日、人種、性別、悪性黒色腫が生じた部位、がんの広がり、BRAF遺伝子変異の種類、PD-L1発現の有無、採血データ、術後補助療法などの治療歴、病期、使用された薬剤、治療期間、治療効果、副作用の発生状況、再発や生存の有無、等が含まれます。 4.外部への情報の提供と情報の保存、管理、二次利用 研究代表施設へのデータの提供は、氏名、カルテ番号等の直ちに個人が判別できる情報が消去された状態で、電子メールやインターネット上の共有フォルダを介してやり取りされます。対応表は、各施設の研究責任者が保管・管理します。 〇情報の保存、二次利用 この研究に使用した情報は、研究の中止または研究終了後5年間まで、札幌医科大学皮膚科学講座のパスワード等で管理・制御されたコンピューターに保存します。また、この研究以外の目的で使用されることはありません。 〇情報の管理責任者:この研究で使用する情報は、札幌医科大学附属病院 皮膚科 宇原久が管理します。 〇上記の事柄についての情報を公開している期間(オプトアウト期間): 2022年2月28日まで 5.研究組織 【研究統括者】 国立がん研究センター中央病院皮膚腫瘍科 科長 山﨑 直也 【研究代表者 ・ 研究事務局 ・ 代表施設の研究責任者 ・ 解析担当者】 国立がん研究センター中央病院皮膚腫瘍科 医長 並川 健二郎 【共同研究機関名 / 各機関の研究責任者】 北海道大学 形成外科 前田 拓、 旭川医科大学 皮膚科 松谷 泰佑、札幌医科大学 皮膚科 宇原 久 、筑波大学 皮膚科 藤澤 康弘、埼玉県立がんセンター 皮膚科 大芦 孝平、埼玉医科大学国際医療センター 皮膚腫瘍科・皮膚科 中村 泰大 、埼玉医科大学 皮膚科 柳澤 宏人 、がん・感染症センター都立駒込病院 皮膚腫瘍科 吉野 公二、 慶應義塾大学 皮膚科 舩越 建、 東京大学 皮膚科 宮川 卓也、 新潟県立がんセンター新潟病院 皮膚科 竹之内 辰也 、富山県立中央病院 皮膚科 八田 尚人、 信州大学 皮膚科 木庭 幸子 、静岡がんセンター 皮膚科 吉川 周佐 、京都府立医科大学 皮膚科 浅井 純 、大阪国際がんセンター 腫瘍皮膚科 爲政 大幾 、国立病院機構九州がんセンター 皮膚腫瘍科 内 博史、 福岡大学 皮膚科 筒井 啓太、 九州大学 皮膚科 伊東 孝通、 久留米大学 皮膚科 武藤 一考、 熊本大学 皮膚科 福島 聡、 鹿児島医療センター 皮膚腫瘍科・皮膚科 松下 茂人、 千葉大学 皮膚科 猪爪 隆史、 名古屋市立大学 加齢・環境皮膚科 加藤 裕史、 自治医科大学 皮膚科 前川 武雄、 岡山大学 皮膚科 山﨑 修、 神戸大学 皮膚科 中野 英司 6.お問い合わせ先 本研究に関するご質問等がありましたら下記の連絡先までお問い合わせ下さい。 ご希望があれば、他の研究対象者の個人情報及び知的財産の保護に支障がない範囲内で、研究計画書及び関連資料を閲覧することが出来ますのでお申出下さい。 また、情報が当該研究に用いられることについて患者さんもしくは患者さんの代理人の方にご了承いただけない場合には研究対象としませんので、下記の連絡先までお申出ください。その場合でも患者さんに不利益が生じることはありません。 当院におけるお問い合わせ窓口 〒060-8556 札幌市中央区南1条西17丁目
札幌医科大学附属病院 皮膚科 教授 宇原久 平日 TEL 011-611-2111 内線 34550(教室) 夜間休日 TEL 011-611-2111 内線 34620(9階北病棟看護室)
⑰ 公開文書: 露光部(非粘膜型/非末端黒子型)メラノーマにおけるニボルマブ+イピリムマブ併用療法の一次治療と抗PD-1抗体単剤療法の一次治療(無効後ニボルマブ+イピリムマブを含む)の効果に関する多施設共同後ろ向き研究
2021年 11月 22日 皮膚科 患者の皆様へ 現在、皮膚科では、メラノーマ治療薬(抗PD-1抗体あるいは抗PD-1抗体 + 抗CTLA-4抗体の併用療法)の効果と副作用を検討する研究を行っています。今後の治療に役立てることを目的に、この研究では2014年7月~2021年7月に当院で抗PD-1抗体あるいは抗PD-1抗体 + 抗CTLA-4抗体の併用療法を受けられた患者さんの診療情報などを利用させて頂きます。診療情報などがこの研究で何のために、どのように使われているのかについて詳しく知りたい方は、下記の窓口にご連絡ください。 1.研究課題名 「露光部(非粘膜型/非末端黒子型)メラノーマにおけるニボルマブ+イピリムマブ併用療法の一次治療と抗PD-1抗体単剤療法の一次治療(無効後ニボルマブ+イピリムマブを含む)の効果に関する多施設共同後ろ向き研究」 2.研究の意義・目的
「治療選択に関する有益な情報が少ない本邦の露光部メラノーマの治療選択において、有用な情報を得る」 3.研究の方法
「承認の日から2024年3月31日の間において、対象となる患者の年齢、性別、既往歴、併存疾患、原発巣部位、病期、再発・転移部位、先行治療の有無と種類、先行した抗PD-1抗体の使用回数と種類、ニボルマブ+イピリムマブ併用療法の使用回数、後治療の有無と種類、治療を受けた後の全生存率、治療を受けた後の無増悪生存率、治療の奏効率、全観察期間、有害事象とその程度、BRAF 変異の有無(BRAF変異とはメラノーマの増殖をつかさどる遺伝子変異のことです)、PD-L1発現の有無(PD-L1はがん細胞が出している、がんを攻撃しにやってきたTリンパ球を抑制する分子です),血液・生化学検査データ、組織所見などを調査する」 全体の参加施設数 19施設、全体の目標症例数 200例 当院の参加症例数 10例 4.個人情報の取り扱いについて 本研究で得られた個人情報は、匿名化して管理し外部に洩れることのないように厳重に管理します。研究成果の発表にあたっては、患者さんの氏名などは一切公表しないこととします。データ等は、患者さんが治療を受けた医療施設や、そのデータを集めて解析する千葉大学大学院医学研究院皮膚科研究室、埼玉医科大学国際医療センター
皮膚腫瘍科・皮膚科、それぞれの鍵のかかる保管庫で保管します。 5.外部への試料・情報の提供
匿名化されたデータは研究を統括する千葉大学大学院医学研究院皮膚科研究室に集めら れ、さらに統計解析機関の埼玉医科大学国際医療センター皮膚腫瘍科・皮膚科へ送られ、 解析されます。対応表は患者さんが治療を受けた医療施設の研究責任者が保管・管理し、 外部に送られることはありません。6.研究組織
統括研究施設および代表研究者
千葉大学大学院医学研究院皮膚科学 猪爪隆史 共同研究施設および研究責任者 埼玉医大国際医療センター 皮膚科・皮膚腫瘍科 中村泰大; 国立がん研究センター中央病院 皮膚腫瘍科 並川健二郎 ;静岡県立静岡がんセンター 皮膚科 吉川周佐; 自治医科大学 皮膚科 前川武雄; 新潟県立がんセンター新潟病院 皮膚科 竹之内辰也 ;信州大学 皮膚科 木庭幸子; 群馬大学 皮膚科 安田正人; 名古屋市立大学 皮膚科 加藤裕史; 大阪国際がんセンター 腫瘍皮膚科 爲政大幾; 岡山大学 皮膚科山崎 修; 熊本大学 皮膚科 福島 聡; 国立病院機構鹿児島医療センター 皮膚腫瘍科 松下茂人 ;札幌医科大学 皮膚科 宇原 久 ;筑波大学 皮膚科 藤澤康弘 ;がん・感染症センター都立駒込病院皮膚腫瘍科 吉野公二; 九州大学 皮膚科 伊東孝通; 京都府立大学 皮膚科 浅井 純 ;三重大学 皮膚科 北川敬之 7.研究に診療情報などを利用して欲しくない場合について ご協力頂けない場合には、原則として結果の公開前であれば情報の削除などの対応をしますので、下記の窓口にご遠慮なくお申し出ください。文部科学省・厚生労働省による「人を対象とする生命科学・医学系研究に関する倫理指針」に基づいて掲示を行っています。研究実施機関:札幌医科大学医学部皮膚科学講座 本件のお問合せ先:札幌医科大学皮膚科学教室 教授 宇原久 〒060-8556 札幌市中央区南1条西17丁目 電話(011)-611-2111 内線 34550 (皮膚科教室) FAX (011)-613-3739 平日 午前9時~午後5時 上記以外の時間(夜間・休日)は、 札幌医科大学附属病院9階北病棟 電話(011)-611-2111 内線 34620 研究代表機関 :千葉大学大学院医学研究院皮膚科学 研究代表者:猪爪隆史
⑱ 爪甲色素線条画像データセットの構築
「爪甲色素線条画像データセットの構築」に関する臨床研究に臨床画像の提供を行っています。 信州大学医学部医倫理委員会の審査による医学部長の承認を得て実施しています。 1.研究課題名: 爪甲色素線条画像データセットの構築 2.所属(診療科等): 信州大学医学部皮膚科 3.研究責任者(職名): 皆川茜(助教)4.研究実施期間: 倫理委員会承認日~2026年8月31日 5.研究の意義、目的: 爪甲色素線条の客観的指標の確立に関する学術的研究活動促進のために、爪甲色素線条のダーモスコピー画像のデータを収集、蓄積しデータセットを構築し、爪部悪性黒色腫の診断補助プログラム検証のための臨床性能試験に用いる。(臨床性能試験の詳細は研究計画書を別途作成予定)6.対象となる患者さん: 2007年1月1日以降に爪甲色素線条の拡大写真(ダーモスコピー写真という、カメラを皮膚に密着して撮影する特殊な写真)を撮影された方 7.利用する診療記録/検体: 臨床画像、良悪性情報、生検の実施有無、生検実施年月日、性別、生年月日、部位、画像撮影年月日、撮影機器 8.他機関への試料・情報の提供方法: EDCシステム(電子的配信)および登録票に記載して提供します 9.研究方法: 後ろ向きデータ収集 10.研究機関名: 信州大学医学部皮膚科 (責任者:皆川茜) 11. 問い合わせ(信州大学)主任施設の名称:信州大学研究責任者 皆川茜 問い合わせ(当院)氏名(所属・職名):講師 神谷崇文 電話: 011-611-2111 既存の画像や診療記録を研究、調査、集計しますので、新たな診察や検査、検体の採取の必要はありません。利用する情報からは、患者様を直接特定できる個人情報を削除し、信州大学皮膚科に提供します。 研究成果は今後の医学の発展に役立つように学会や学術雑誌などで発表します。また将来的に医療機器等の開発に用いることがあります。しかし、その際も患者様を特定できる個人情報は利用しません。 また収集する情報の精査過程において、カルテなどの診療情報を信州大学の本研究の担当者が閲覧させていただくことがあります。その場合も、個人情報の取り扱いには十分配慮し、外部に個人情報を持ち出すことはありません。 この研究にご自分の診療記録等を利用することをご了解いただけない場合、またご不明な点については、上記問い合わせ先までご連絡くださいますようお願いいたします。 画像利用への不参加を申し出られた場合でも、なんら不利益を受けることはありません。ただし、同意取り消しの申し出をいただいたとき、すでに研究成果が論文などで公表されていた場合や、試料や情報が匿名化されて個人が全く特定できない場合などには、結果を廃棄できないこともあり、引き続き使わせていただくことがあります。 不同意の場合には、 以下各病院で選択 a.当院に「試料等の研究目的利用に関する不同意書」をご用意しておりますので、これに必要事項をご記入の上、札幌医科大学皮膚科教室宛てにご提出ください。 b.当院皮膚科主治医までご連絡ください。
⑲ 公開文書:新規乾癬患者の疫学調査
西暦 2022 年 4 月~2026 年 3 月に乾癬で当院を受診される方へ 作成日: 2022 年 1 月 14 日(第 1.0 版)1 研究について この研究を実施することについては、名古屋市立大学医学系研究倫理審査委員会(所在地:名古屋市瑞穂区瑞穂町字川澄1)において医学、歯学、薬学その他の医療又は研究に関する専門家や専門以外の方々により倫理性や科学性が十分であるかどうかの審査を受け、承認されたうえで、研究を実施する研究機関の長から研究を実施することについての許可を受けています。また委員会では、この研究が適正に実施されているか継続して審査を行います。 なお、本委員会にかかわる規程等は、以下のホームページよりご確認いただくことができます。 名古屋市立大学病院臨床研究開発支援センター ホームページ “患者の皆様へ” http://ncu-cr.jp/patient 2 本研究施設における研究責任者の氏名および研究分担者の氏名 研究機関名: 札幌医科大学 皮膚科学講座 研究責任者: 教授 ・ 宇原 久 研究分担者: 肥田 時征、神谷 崇文 なお、この研究は、多機関共同研究であるため、以下の研究機関が参加しています。 【研究代表者】 研究機関名: 名古屋市立大学大学院医学研究科 加齢・環境皮膚科 研究代表者: 教授 ・ 森田 明理 【共同研究機関】 研究機関名 日本乾癬学会に関連する全国の乾癬診療を行う病院 116 施設 多数の機関であり詳細はお問い合わせによりお答えすることができます 3 研究の目的、意義 現在わが国の乾癬患者数は 10 万人以上と推定され、近年生活の欧米化に伴い患者数は年々増加傾向にあります。新規乾癬患者の実態の把握は治療発展には不可欠なデータで、乾癬患者さんのデータを収集し、今後の乾癬治療の発展に寄与したいと考えています。 この研究で用いる情報は診療録から得られる、乾癬の病型・皮疹の部位・年齢・性別、その他の医療情報です。乾癬登録ケースカードへ情報を記入し、年間の新規乾癬患者数、性別、病型、治療内容などの傾向を明らかにし、今後の治療や患者指導に役立てることを目的としています。集計結果は日本乾癬学会学術総会にて報告します。乾癬登録ケースカードによって得られた新規乾癬患者の情報をもとに、医療現場の希求する、よりよい乾癬治療薬、治療法の開発、患者に対する的確な指導が可能になります。 4 あなたがこの研究の対象者として選定された理由 以下の項目の全てが当てはまる方に、この研究に参加していただけます。 ① 西暦 2022 年 4 月 1 日から西暦 2026 年 3 月 31 日までに各研究機関に受診し乾癬と診断された方 5 この研究の方法及び期間 西暦 2022 年 4 月 1 日から西暦 2026 年 3 月 31 日までに各研究機関に受診し乾癬と診断された方を対象とし、その医療情報を用います。用いる医療情報は、診療録から得られる情報で、臨床写真は含みません。これらの医療情報は乾癬登録ケースカードに記載し、記載されたケースカードを年度毎に集計し、その集計結果を日本乾癬学会学術総会で報告します。この研究のために費用負担が発生することはありません。また、予測されるリスク・利益ともにございません。 6 あなたがこの研究に参加することによって期待される利益と予測される負担やリスク ≪利益について≫ あなたがこの研究に参加されますと、医学の進歩に貢献していただいたことになります。 ≪不利益(負担やリスク)について≫ この研究のために費用負担やリスクが発生することはありません。 7 同意の撤回の自由について この研究への参加はあなたの自由意思によるものです。この研究に同意された後であっても、参加を取りやめることができます。同意の撤回を希望する場合は、主治医にその旨を伝えてください。同意を撤回された後は、あなたの試料・情報は取り除きます。ただし、研究の進捗状況によっては、個人情報の特定ができない状態に既に加工されていることがあり、その場合はあなたのデータを取り除くことができないことがあります。 8 研究への参加に同意しなくても、途中で同意を撤回しても、不利益な取り扱いを受けることはありません。 あなたがこの研究への参加に同意されない場合や、途中で参加をとりやめる場合でも、今後の治療等で決して不利益を受けることはありません。 9 研究計画書及び研究の方法関する資料の入手または閲覧できる旨、その方法 研究計画書は閲覧可能ですので、ご覧になりたい方は研究責任者もしくは研究分担者にお申し出ください。また、この研究が終了して研究の結果がまとめられた後、あなたの希望があれば、この研究の結果をお知らせすることができます。 10 個人情報等の取り扱い あなたの試料・情報は、それらから住所、氏名等の個人を特定する情報が削られ、代わりに新しく符号がつけられて匿名化します。なお、あなたとこの符号とを結びつける対応表は、 あなたの試料・情報を頂いた病院や研究機関で厳重に保管します。 11 試料・情報の保管方法、廃棄方法 この研究の試料・情報については、研究期間中、施錠可能な場所に研究責任者が保管します。電子媒体の情報は、PC 上に保管し、ファイルにパスワードをかけて、施錠可能な場所に保管します。これらの試料・情報は、この研究の終了について報告した日から5年を経過した日、またはこの研究の結果の最終の公表について報告した日から3年を経過した日のいずれか遅い日までの期間保管されます。 研究終了後、保管期間が経過した場合、試料・情報は廃棄します。このとき、紙媒体の資料は、シュレッダーで裁断し、再現不可能な状態にした上で廃棄し、書き換え不可能な電子媒体の場合、物理的に破壊してデータ読み取りを不可能にした上で、適切に廃棄します。また、書き換え可能な電子媒体のデータの場合、物理的に破壊してデータ読み取りを不可能にするか、又はダミーデータを複数回上書きして元のデータを復元不可能な状態にした上で、同様に廃棄します。あなたが同意を撤回した場合、その時点で同様に紙媒体及び電子媒体の資料を廃棄します。12 あなたから頂いた試料・情報について、将来の他の研究に用いられる可能性、又は他の研究機関に提供する可能性 保管した検体を、将来、乾癬患者さんの疫学調査に関する研究に使用させていただくことが予想されます。その場合には、改めて医学系研究倫理審査委員会にその研究の研究計画書を提出し承認を受けます。研究に用いるデータは既に匿名化され、誰のものか判別できないように加工されているため、改めて同意を取得することはございません。 13 研究により得られた結果等の取り扱い この研究が終了して研究の結果がまとめられた後、あなたの希望があれば、この研究の結果をお知らせすることができます。 14 研究についてのご相談、健康状態に問題があると感じられたときの医療機関の連絡先 この研究について知りたいことや、ご心配なことがありましたら、遠慮なくご相談ください。 【問い合わせ先】 研究実施機関: 札幌医科大学 皮膚科学講座 連絡先: 011-611-2111 (対応可能時間帯) 9 時 00 分から 17 時まで(平日) 対応者: 札幌医科大学 皮膚科学講座 助教 熊谷 綾子 研究代表者: 名古屋市立大学大学院医学研究科 加齢・環境皮膚科 教授 森田 明理 15 あなたに対する費用負担、謝礼の有無 この研究は、あなたが日常で行っている治療や検査の結果などのデータを拝見させていただく研究であるため、あなたに新たな費用の負担を求めることはありません。 この研究に参加いただくことによる謝礼はありません。 16 他の治療方法等について この研究は日常の診療で行う検査等のデータを観察する研究ですので、この研究に参加しても参加しなくても行う治療は同じです。 17 研究実施後の医療の提供に関する対応 この研究に参加していただいた後の治療等に制限はありません。 18 研究によって生じた健康被害に対する補償の有無、その内容 この研究の参加中に、本研究に参加したことにより健康被害を受けた場合は、通常の診療と同様に適切に対処します。その際の医療費は、あなたが加入している健康保険の自己負担額についてはお支払いいただくことになります。本研究は医療情報を用いる研究であるため、この研究による健康被害はありません。臨床研究保険には加入せず、研究の実施に伴い生じた健康被害に対する医療の提供のみを行います。健康被害の発生により、損害保険による補償金が支払われることはありません。 19 この研究の資金源及び利益相反(COI(シーオーアイ):Conflict of Interest)について 研究一般における、利益相反(COI)とは「主に経済的な利害関係によって公正かつ適正な判断が歪められてしまうこと、または、歪められているのではないかと疑われかねない事態」のことを指します。具体的には、企業等が研究に対してその資金を提供している場合や、研究に携わる研究者等との間で行われる株券を含んだ金銭の授受があるような場合です。このような経済的活動が、研究の結果を特定の企業や個人にとって有利な方向に歪曲させる可能性を判断する必要があり、そのために研究の資金源や、各研究者の利害関係を申告することが定められています。 この研究は、日本乾癬学会から資金提供を受けて実施します。 なお、この研究では、企業等の関与と、研究責任者および研究分担者等の利益相反申告が必要とされる者の利益相反(COI)について、札幌医科大学利益相反管理委員会の手続きを終了しています。 20 研究成果の帰属について この研究で得られるデータ又は発見に関しては、日本乾癬学会が権利保有者となります。この研究で得られるデータを対象とした解析結果に基づき、特許権等が生み出される可能性がありますが、ある特定の個人のデータから得られる結果に基づいて行われることはありません。したがって、このような場合でも、あなたが経済的利益を得ることはなく、あらゆる権利は、研究者もしくは研究者の所属する研究機関にあることをご了承ください。 21 一部業務の委託機関について データマネジメントについて下記企業に委託しております。各施設で収集した情報を下記企業へ送付しますが、その際には匿名化した情報を送ります。そのため、あなたの個人情報が企業へ送られることはありません。 アポプラスステーション株式会社 CRO 事業部 施設責任者:小山 佳克
⑳ 2011年1月1日から2021年12月31日までの期間に札幌医科大学附属病院にて足底のメラノーマ患者の治療を受けられた方へ
―「当院における足底メラノーマの発症部位の検討」へご協力のお願い―
研究機関名: 札幌医科大学附属病院; 研究機関長病院長: 土橋和文 ; 研究責任者: 札幌医科大学附属病院皮膚科 助教 加藤潤史 1.研究の概要 1) 研究の目的 日本人のメラノーマの約3-4割が足底に生じます。足底の中でも踵は荷重が強くかかる部位ですが、土踏まずは非荷重な部位となります。札幌医科大学附属病院皮膚科において足底メラノーマの治療を受けられた方の発症部位と腫瘍の厚さなどを調べて、発症部位と腫瘍の厚さ(進行度)の実態を把握することにより、非荷重部のメラノーマの発症率を把握し、荷重がメラノーマの発症に関わっているかどうかを明らかにすることがこの研究の目的です。 2) 研究の意義・医学上の貢献 これまで札幌医科大学附属病院皮膚科で足底メラノーマの治療を受けられた方の結果を把握する事により、荷重がメラノーマの発症に関わっているかどうかを明らかにすることで今後のメラノーマの診断や治療後のケアの改善に貢献できる可能性があります。 2.研究の方法 1) 研究対象者 2011年1月1日から2021年12月31日の間に札幌医科大学附属病院皮膚科において足底の治療を受けられた方が研究対象者です。 2) 研究期間 病院長承認後~2025年12月31日 3) 予定症例数50人を予定しています。 4) 研究方法 2011年1月1日から2021年12月31日の間に札幌医科大学附属病院皮膚科において足底の治療を受けられた方で、研究者が診療データ(診療録、写真、病理報告書)をもとに、発生部位と腫瘍の厚さについて調べます。 5) 使用する情報 この研究に使用するのは、大学病院の診療データ(診療録、写真、病理報告書)の情報の中から発症部位、腫瘍の厚さ、年齢、性別の項目を抽出し使用させていただきます。氏名、生年月日などのあなたを特定できる情報は削除してあなたの情報などが漏洩しないようプライバシーの保護には細心の注意を払います。 6) 情報の保存、二次利用 この研究に使用した情報は、研究の中止または研究終了後、研究完了(中止)報告書を提出した日から5年が経過した日までの間、パスワードで管理・制御されたコンピューターに保存します。その情報は皮膚科学講座の教室内の施錠可能な保管庫に保存します。なお、この研究に使用した情報を将来の別の研究に利用する可能性はありません。 7) 情報の管理について責任を有する者の氏名又は名称 札幌医科大学附属病院 病院長 土橋和文 8)研究結果の公表 この研究の結果は学会や論文で発表します。その際も氏名、生年月日などのあなたを特定できるデータは一切含まないようにします。 9) 研究に関する問い合せ等 この研究にご質問等がありましたら下記の連絡先までお問い合わせ下さい。 また、あなたの情報が研究に使用されることについて、あなたもしくは代理人の方にご了承いただけない場合には研究に使用しませんので、2023年12月31日までの間に下記の連絡先までお申し出ください。お申し出をいただいた時点で、研究に用いないように手続をして、研究に用いられることはありません。この場合も、その後の診療など病院サービスにおいて患者さんに不利益が生じることはありません。ご連絡頂いた時点が上記お問い合せ期間を過ぎていて、あなたを特定できる情報がすでに削除されて研究が実施されている場合や、個人が特定できない形ですでに研究結果が学術論文などに公表されている場合は、解析結果からあなたに関する情報を取り除くことができないので、その点はご了承下さい。 連絡先 札幌医科大学附属病院 皮膚科学講座 助教 加藤潤史 <平日> TEL 011-611-2111 内線 34550(教室) 9時00分~17時00分 <夜間・休日・時間外> TEL 011-611-2111 内線 34620(9階北病棟看護室)
21 シミに対する治療を受けられた患者さん・ご家族の皆様へ
札幌医科大学皮膚科 学講座(以下、当科)では、「臨床写真に基づく深層学習を活用した皮膚疾患画像分析~シミの鑑別への応用~」 という臨床研究を行っています。そのため、当科でシミに対する治療を受けられた患者様の診療情報を使用させていただきますので、以下の内容を確認してください。なお、この研究は、近畿大学医学部倫理委員会(https://www.med.kindai.ac.jp/rinri/index.html)で審査・承認を受け、札幌医科大学附属病院病院長による実施の許可を受けて行われます。 1. 情報の利用目的及び利用方法 一般的にシミと呼ばれる病変にはさまざまな疾患が含まれます。この研究では、AIを用いてこれらの疾患が鑑別できるかを検証することを主な目的としています。そのため、2014年4月1日~2024年3月31日の間に当科でシミに対する治療を受けられた患者さんを対象として、診療情報のみを研究に利用します。利用する情報は、患者さん個人が特定されないようにした上で、個人情報に関しては、厳重に管理します。なお、それらの情報を他の機関へ提供することはありません。本研究で取得した情報を将来別の研究の用いる可能性がありますが、その際は改めて倫理委員会での審査を受けます。2. 利用し、又は提供する情報の項目 診療情報(年齢、性別、診断名、治療歴、診察記録、臨床写真) なお、当該情報は診療録より収集します。 分担研究施設においては、診断名と臨床写真のみ収集します。 3. 利用又は提供を開始する予定日 病院長による実施許可日(2024年10月29日)から開始します。 4. 情報の提供を行う機関の名称及びその長の氏名 近畿大学医学部 医学部長 松村 到、 札幌医科大学附属病院 病院長 渡辺 敦、 京都大学医学部 医学部長 伊佐 正、 愛媛大学医学部 医学部長 羽藤 直人、 かねとも皮フ科クリニック 院長 金友 仁成、 医療法人 葛西形成外科 理事長 葛西 健一郎 5. 提供する情報の取得の方法 診療録(電子カルテ等)より取得し、札幌医科大学皮膚科により研究代表機関である近畿大学医学部へ提供されます。上記の研究施設より得られた診断名と臨床写真は、診療録から得られた個人の氏名、生年月日などの個人を識別できる情報を削除して適切に取り扱います。追跡可能なレターパックにより、研究代表機関である近畿大学医学部へ提供されます。 6. 提供する情報を用いる研究に係る研究責任者(多機関共同研究にあっては、研究代表者)の氏名及び当該者が所属する研究機関の名称 近畿大学医学部皮膚科学教室 大塚 篤司 7. 利用する者の範囲 本研究に携わる近畿大学医学部皮膚科学教室の医師 大塚 篤司・中嶋 千紗・山本 晴代・三宅 早苗・渡辺 圭子・山村 優人・森田 駿介・ 高田 真衣・谷崎 英里香・飯沼 紀実 解析を行う機関の研究者:近畿大学工学部電子情報工学科 竹田 史章 8. 情報の管理について責任を有するものの名称 近畿大学医学部、札幌医科大学、京都大学医学部、愛媛大学医学部附属病院、かねとも皮フ科クリニック、医療法人 葛西形成外科、近畿大学工学部 9. 研究対象者等の求めに応じて、研究対象者が識別される情報の利用又は他の研究機関への提供を停止する旨 この研究では、患者さん・ご家族の診療情報が利用されることに同意できず、拒否されたい場合に、下記の方法により、いつでもその利用を停止することが可能です。また、利用の停止を受け付けた場合でも、その後の診療において一切の不利益を受けることはありません。なお、申し出のタイミング(論文・学会発表等による公表後)によっては、利用を停止できない場合もあります。10. 9の研究対象者等の求めを受け付ける方法 下記までご連絡ください。なお、この研究に関するすべてのお問い合わせも下記で受け付けます。 [お問い合わせ先] 札幌医科大学附属病院 皮膚科 (宇原 久・佐藤さゆり) 電話:011-611-2111(土日祝日を除く8:30~17:30)
| 月 | 火 | 水 | 木 | 金 | |
| 1 | 2 | 3 | 4 | 5 | |
| 新来担当 | 肥田 | 松井 | 箕輪 | 熊谷 | |
| 再来担当 | 箕輪 | 細川 | 堀本 | 肥田 | 菅 |
| 熊谷 | 佐藤 | 加藤 | 松井 | 静川 | |
| 楢崎 | 大瀧 | 細川 | 阿部貴 | ||
| am阿部 | 前田 | 静川 | |||
| 8 | 9 | 10 | 11 | 12 | |
| 新来担当 | 肥田 | 菅 | 堀本 | ||
| 再来担当 | 箕輪 | 細川 | 堀本 | 細川 | 菅 |
| 熊谷 | 阿部貴 | am加藤 | 前田 | 阿部貴 | |
| 阿部貴 | 大瀧 | 楢崎 | 大瀧 | ||
| am松井 | 佐藤 | ||||
| 15 | 16 | 17 | 18 | 19 | |
| 新来担当 | 肥田 | 箕輪 | 加藤 | 熊谷 | |
| 再来担当 | 箕輪 | 細川 | 堀本 | 肥田 | 菅 |
| 熊谷 | 阿部貴 | 加藤 | 松井 |
楢崎 | |
| 堀本 | am堀本 | 細川 | 佐藤 | ||
| am楢崎 | 前田 | 大瀧 | |||
| 22 | 23 | 24 | 25 | 26 | |
| 新来担当 | 肥田 | 菅 | 加藤 | 堀本 | |
| 再来担当 | 箕輪 | 細川 | 堀本 | 肥田 | 菅 |
| 熊谷 | 前田 | 加藤 | 松井 | 静川 | |
| 佐藤 | 大瀧 | 細川 | 阿部貴 | ||
| am前田 | 楢崎 | 大瀧 |
|
||
| 29 | 30 | ||||
| 新来担当 | 肥田 | ||||
| 再来担当 | 箕輪 | 楢崎 | |||
| 熊谷 | 前田 | ||||
| 前田 | 静川 | ||||
| am大瀧 |
| 月 | 火 | 水 | 木 | 金 | |
| 1 | 2 | 3 | |||
| 新来担当 | 菅 | 加藤 |
堀本 |
||
| 再来担当 | 堀本 | 肥田 | 菅 | ||
| 加藤 | 松井 | 腫瘍チーム | |||
| 阿部史 | 阿部史 |
静川 |
|||
| 前田 | 大瀧 | ||||
| 6 | 7 | 8 | 9 | 10 | |
| 新来担当 | 肥田 | 松井 | 箕輪 | 熊谷 |
|
| 再来担当 | 箕輪 | 細川 | 堀本 | am松井 | 菅 |
| 熊谷 | 楢崎 | am加藤 | 細川 | 阿部史 | |
| 阿部史 | 静川 | 阿部史 | 佐藤 | 楢崎 | |
| 大瀧 | 大瀧 | ||||
| 13 | 14 | 15 | 16 | 17 | |
| 新来担当 | 肥田 | 箕輪 | 堀本 | 熊谷 | |
| 再来担当 | 箕輪 | 細川 |
堀本 | 肥田 | 菅 |
| 熊谷 | 佐藤 | 加藤 | 松井 | 静川 | |
| 阿部史 | 大瀧 | 阿部史 | 阿部史 | 大瀧 | |
| 楢崎 | 阿部貴 | 静川 | |||
| 20 | 21 | 22 | 23 | 24 | |
| 新来担当 | 菅 | 加藤 | 箕輪 | ||
| 再来担当 | 細川 |
堀本 | 松井 | 菅 | |
| 楢崎 | 加藤 | 阿部史 | 阿部貴 | ||
| 佐藤 | 細川 | 静川 | 大瀧 | ||
| 阿部史 | |||||
| 27 | 28 | 29 | 30 | 31 | |
| 新来担当 | 肥田 | 松井 | 菅 | 熊谷 | |
| 再来担当 | 箕輪 | 細川 | 堀本 | 肥田 | 菅 |
| 熊谷 | 佐藤 | 加藤 | 松井 | 阿部貴 | |
| 阿部史 | 静川 | 細川 | 阿部史 | 大瀧 | |
| 阿部貴 | 阿部史 | 楢崎 |
![]() 担当医の変更が生じる場合もございますのでご了承下さい。
担当医の変更が生じる場合もございますのでご了承下さい。