研究
消化管
炎症性腸疾患研究
腸炎関連大腸癌の発癌機序の解明
炎症性腸疾患の罹患患者ならびに長期罹患患者の増加に伴い,腸炎関連大腸癌例も増加しており,その機序解明と治療開発は急務である.われわれは,独自の実験モデルを用いて,腸炎関連大腸癌の浸潤・転移に関わる新たな分子を同定できた(論文投稿中).臨床応用を目指し研究を加速させたいと考えている.
腸上皮幹細胞とニッチの再構築
間葉系幹細胞は骨髄で造血幹細胞のニッチを構成するが,造血幹細胞以外の体性幹細胞とニッチを形成できるかは不明である.最近,われわれは,ラット大腸上皮3次元培養法を独自に開発し,腸管上皮幹細胞に対する間葉系幹細胞のニッチ機能が,腸管上皮の修復・再生に重要であることを明らかにした(論文投稿中).
骨髄-腸管連関の解明
幹細胞移植と炎症性腸疾患の接点は古く,1990年代初頭から基礎研究・臨床試験が報告されているが,腸管組織における由来細胞の分化や細胞運命は不明な点が多い.われわれは,動物モデルを用いてこの骨髄-腸管連関を解明し,それを応用することで,傷害腸管の創傷治癒機転を促進させる新規治療の開発を目指している.
消化管がん研究
消化管(食道・胃・大腸)腫瘍における遺伝子異常の内視鏡診断学への応用
消化管内視鏡検査は食道がん、胃がん、大腸がんの早期発見と治療において極めて重要な検査です。内視鏡診断学が進歩し、病変の表面微細構造、血管形態を詳細に観察することで、がんの存在、病変の範囲、深さ、組織型などを診断することが可能となっております。
内視鏡診断学は詳細な拡大内視鏡所見と病理組織との徹底的な対比から構築されてきました。我々はさらに分子生物学的観点を加えることで、拡大・超拡大内視鏡所見が反映する分子生物学的意義を検討しております。
この研究成果を、例えば『発がんリスクの高い大腸ポリープ』『リンパ節転移リスク』『腫瘍の生物学的悪性度』など、腫瘍の分子生物学的特性を考慮した分子イメージングも含めた内視鏡診断に応用することを目指したtranslational researchを展開しております。
消化管がんの発がんリスク・超早期診断法の実用化に向けた研究
胃がん、大腸がんの発生において、ヒストン修飾やDNAメチル化異常などのエピゲノム異常が重要な役割を担っております。エピゲノム異常が正常の胃・大腸粘膜に蓄積して発がん素地を形成し、がん化に寄与していることが明らかとなっています。
そこで我々は胃・大腸粘膜におけるエピゲノム異常を明らかとし、発がんリスク予測、発がん予防、超早期診断への臨床応用を目指した研究を行っております。これまでに胃がんのリスクマーカーとして有用な遺伝子を同定し、また大腸でも大腸鋸歯状病変の背景粘膜を中心に精力的に研究を行っております。
消化器癌の分子診断・治療のバイオマーカーとしてのノンコーディングRNAの重要性
ノンコーディングRNAはタンパク質へ翻訳されずに機能するRNAの総称であり、特定のDNAに直接作用、またはRNAやタンパク質と相互作用することで、遺伝子発現やエピゲノム異常に関わっていることが近年の研究で明らかにされています。消化器癌においては様々な癌種においてノンコーディングRNAの一種であるマイクロRNAの発現異常が報告され、診断や治療のバイオマーカーになる可能性が示唆されています。これまでに我々は胃癌や大腸癌、消化管GIST、直腸カルチノイド、肝臓癌、膵癌の組織検体を用いた検討でバイオマーカーとして将来的に臨床応用可能なマイクロRNAを多数同定してきました。またノンコーディングRNAは患者の血漿や血清、糞便などからも抽出できることから非侵襲的なLiquid Biopsyとして臨床応用できる可能性もあります。よって現在、我々は消化器癌の超早期診断や分子標的薬剤などの効果予測因子の新規バイオマーカーとしてノンコーディングRNAを用いた非侵襲的分子診断方法の開発を目指し、研究を進めております。
腸内フローラと発がんに関する研究
ヒトマイクロバイオーム解析(生物環境を構成する微生物群ゲノムの総称)により健常人の常在菌のゲノム情報が明らかとなりつつあり、腸内細菌叢の変化と発がんの関連が国内外から多数報告されています。大腸がんにおいてもFusobacterium感染が大腸がん発生に関与している可能性が報告されており、我々も大腸がんにおけるエピゲノム異常とFusobacteriumとの興味深い相関を報告しています。しかし大腸発がんにおける腸内細菌叢の役割は、まだ十分解明されていません。
一方、胃がんにおいてはヘリコバクターピロリ感染により誘発される分子異常についての解明が進み、除菌による胃がん予防が実用化されています。
我々は消化器癌発生におけるマイクロバイオーム役割、宿主の腸管免疫に関わる遺伝子などを明らかにすることで、その発癌メカニズムの解明だけでなく、サーベイランスや除菌治療など多岐にわたる分野においての臨床応用可能を目指した研究を行っております。
消化器癌における常在微生物群ゲノム解析と分子異常・生命予後との関連
近年、網羅的遺伝子解析技術の進歩によりヒトの体内に膨大に存在するmicrobiome(生物環境を構成する微生物群ゲノムの総称)と各疾患の関連についての研究が急速に発展している。ヒトの体内にはヒトゲノムの10倍以上のmicrobiomeが存在するといわれており、その多くはヒトの腸管内に存在し、腸内細菌叢を構成していると考えられている。その中でもFusobacterium属は最近、大腸発癌との関連性が明らかとなり、マイクロサテライト不安定性大腸癌で特異的に高発現することが報告されている(参照論文1、2、3)。
一方、膵癌においては歯周病の原因菌と考えられている口腔内常在菌のPorphyromonas gingivalisがその発癌に関与することが近年、明らかとなり、その感染経路として血流や経胆道によるルート、あるいは消化管から逆行性に菌が膵組織へ到達する可能性が示唆されている。このように大腸癌だけでなく、様々な消化器癌におけるmicrobiomeの役割を明らかにすることは、その発癌メカニズムの解明だけでなく、サーベイランスや除菌治療など多岐にわたる分野において臨床応用可能と考えられる。しかしながら多症例の消化器癌臨床検体を用いたmicrobiomeの検討は国内外を問わず、ほとんどなされていないのが現状である。
我々は最近、大腸癌のmicrobiome解析において、共同研究先である米国のダナファーバー癌研究所と協力し、そのFormalin-Fixed Paraffin-Embedded(FFPE)標本を用いた最適な解析方法の開発に成功。このFFPE標本を用いた方法によって、我々はより多くの臨床検体でのmicrobiome解析が可能になった(参照論文2)。それに加え、解析できる対象が前癌病変や早期癌のような微小検体にまで広がったことは発癌早期におけるその役割を解明する上でも非常に重要であると思われる。
そこで我々は札幌医科大学付属病院と関連施設で内視鏡的・外科的に切除された1000症例をこえる消化器癌(食道癌、胃癌、大腸癌、膵癌、胆道癌)を対象とした。それらの臨床検体(FFPE標本)を用いて,16S rRNAシークエンス解析による微生物腫の同定を行った。さらに同定された菌に関しては生命予後や他の臨床病理学的因子、分子異常(遺伝子変異やDNAメチル化の異常、microRNA発現等)との関連について検討した。
16S rRNAシークエンス解析の結果、腸管と口腔内の常在菌であるFusobacterium属が同定され、消化器発癌に関与している可能性が考えられた。大腸癌組織におけるFusobacterium属はこれまでの凍結標本を用いたこれまでの報告とほぼ同じく、その56%(286/511)で検出された。また欧米人の報告と同様に日本人の大腸癌でもマイクロサテライト不安定性大腸癌で特異的に高発現することも明らかとなった(P <0.0001)(参照論文3)。またその他の消化器癌でも食道腺癌の62%(40/65)、胃癌の38%(78/208)、膵癌の9%(25/283)、胆道癌の12%(3/25)でそれぞれFusobacterium属は同定された(図1)。
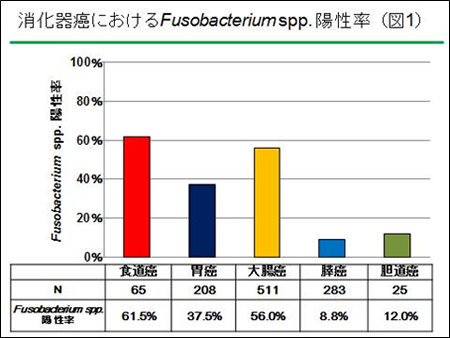
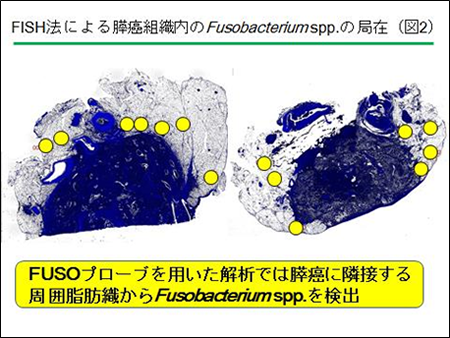
16S rRNAシークエンス解析の結果、腸管と口腔内の常在菌であるFusobacterium属が同定され、消化器発癌に関与している可能性が考えられた。大腸癌組織におけるFusobacterium属はこれまでの凍結標本を用いたこれまでの報告とほぼ同じく、その56%(286/511)で検出された。また欧米人の報告と同様に日本人の大腸癌でもマイクロサテライト不安定性大腸癌で特異的に高発現することも明らかとなった(P <0.0001)(参照論文3)。またその他の消化器癌でも食道癌の61.5%(40/65)、胃癌の37.5%(78/208)、膵癌の8.8%(25/283)、胆道癌の12%(3/25)でそれぞれFusobacterium属は同定された。膵癌組織でのFusobacterium属の報告は皆無であったため、その存在部位を明らかにするためにFISH法を施行。その結果、Fusobacterium属は膵癌組織の近傍の脂肪組織に認められることが明らかとなった(図2)。
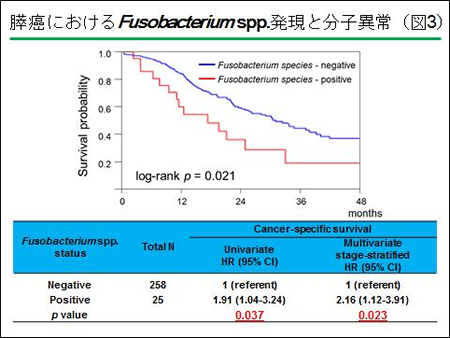
膵癌の分子異常に関する検討ではKRAS変異陽性は膵癌の68%、マイクロサテライト不安定性癌は0%、CpG island methylator phenotype(CIMP)陽性癌は12%、microRNA-21高発現は40%、microRNA-31高発現は32%で認められたが、いずれもFusobacterium属との相関はなかった。一方,Fusobacterium属の陽性群は多変量解析で不良な予後と有意な相関を示した(hazard ratio: 2.16; 95% confidence interval: 1.12−3.91; P = 0.023) (図3)。
今回の検討でFusobacterium属は膵癌組織周囲の脂肪組織内に存在することが明らかとなった。またその陽性群は不良な生命予後との相関が認められたことからFusobacterium属が膵癌の生物学的悪性度に関与する可能性も示唆された(参照論文4)。このように多症例の消化器癌を用いてゲノム解析で同定された微生物種とその分子異常、さらに環境因子との関連を検討することは、将来的に膵癌の新たな予防法や診断・治療法に繋がる可能性があり、消化器癌の新たな治療戦略を世界に先駆けて報告できるものと思われる。よって膵癌におけるmicrobiome解析の更なる発展が期待される。
参照論文
- Ito M, Kanno S, Nosho K, Sukawa Y, Mitsuhashi K, Kurihara H, Igarashi H, Takahashi T, Tachibana M, Takahashi H, Yoshii S, Takenouchi T, Hasegawa T, Okita K, Hirata K, Maruyama R, Suzuki H, Imai K, Yamamoto H, Shinomura Y. Association of Fusobacterium nucleatum with clinical and molecular features in colorectal serrated pathway. Int J Cancer. 2015;137:1258-68.
- Mima K, Sukawa Y, Nishihara R, Qian ZR, Yamauchi M, Inamura K, Kim SA, Masuda A, Nowak JA, Nosho K, Kostic AD, Giannakis M, Watanabe H, Bullman S, Milner DA, Harris CC, Giovannucci E, Garraway LA, Freeman GJ, Dranoff G, Chan AT, Garrett WS, Huttenhower C, Fuchs CS, Ogino S. Fusobacterium nucleatum and T-cells in colorectal carcinoma. JAMA Oncol. 2015;1:653-61.
- Nosho K, Sukawa Y, Adachi Y, Ito M, Mitsuhashi K, Kurihara H, Kanno S, Yamamoto I, Ishigami K, Igarashi H, Maruyama R, Imai K, Yamamoto H, Shinomura Y. Association of Fusobacterium nucleatum with immunity and molecular alterations in colorectal cancer. World J Gastroenterol. 2016;22:557-66.
- Mitsuhashi K, Nosho K, Sukawa Y, Matsunaga Y, Ito M, Kurihara H, Kanno S, Igarashi H, Naito T, Adachi Y, Tachibana M, Tanuma T, Maguchi H, Shinohara T, Hasegawa T, Imamura M, Kimura Y, Hirata K, Maruyama R, Suzuki H, Imai K, Yamamoto H, Shinomura Y. Association of Fusobacterium species in pancreatic cancer tissues with molecular features and prognosis. Oncotarget. 2015;6:7209-20.
消化管がん化学療法における臨床研究
消化管がん(主に胃がん,大腸がん)における化学療法においては,日常臨床においては国内外のエビデンスに基づいた標準的治療を実践するとともに,より治療効果が高い患者を選定するためのバイオマーカーの探索を自主臨床研究として取り組んでいます.また,国内共同臨床試験に参加し,新たな標準的治療の確立にもつとめています.
<主な自主臨床研究>
- HER2陽性の進行胃癌患者を対象としたカペシタビン+シスプラチン+トラスツズマブ併用療法施行例における血清HER2の変動を検討する観察研究
- 切除不能進行・再発胃がんにおけるSPARC発現状況と二次化学療法としてのnab-paclitaxel療法の有効性との関連を探索する前向き臨床研究
<主な国内多施設共同臨床試験>
- RAS遺伝子(KRAS/NRAS遺伝子)野生型で化学療法未治療の切除不能進行再発大腸癌に対するmFOLFOX6+ベバシズマブ併用療法とmFOLFOX6+パニツムマブ併用療法の有効性及び安全性を比較する第3相無作為化比較試験
ヘリコバクターピロリ除菌後胃がんのリスク因子に関する研究
ヘリコバクターピロリ除菌治療により胃がんが激減すると予測され、理論的には除菌成功後の胃がんスクリーニングは長期間の間隔で施行することが考えられてきた。しかし除菌後に発生する胃がんの存在が指摘され、実臨床では除菌成功後も引き続き内視鏡によるスクリーニング検査を実施している実態がある。除菌後であっても発癌リスク因子を適切に設定することができれば、オーダーメイド的な対応も可能になると考えられる。
われわれはヘリコバクターピロリ感染と胃粘膜におけるメチル化異常に関する検討を行い、除菌前後の相違と発癌の関係を明確化することでリスク因子の探索を試みております。
大腸癌とマイクロサテライト不安定性(MSI)
マイクロサテライト不安定性(microsatellite instability, MSI)は、1~数塩基単位のリピート配列(microsatellite配列)においてリピート数が増減する変異のことで、大腸癌の10%がMSI陽性であり、また遺伝性大腸癌であるLynch症候群(LS)では90%以上がMSI陽性になります。LSは若年、癌家族歴、多発大腸癌、他臓器癌との重複など様々な特徴がありますが、実際にはこのような典型例ばかりではなく、高齢発症で家族歴のないLS症例も少なからず存在することが分かってきました。LSの診断はミスマッチ修復(MMR)遺伝子の胚細胞変異により確定されますが、従来は上記のような特徴をもつ大腸癌の患者さんを対象に(Amsterdam criteriaやBethesda guidelines)まずMSIを調べ、MSI陽性であった場合にMMR遺伝子の変異を解析していました。ところがこの方法では、非典型的なLS症例が見逃される可能性があり、LSは大腸癌全体からみると2-3%と少数ではありますが、適切な介入により予後を改善できる疾患であるため、少しでも見逃しを減らすことが大変重要です。またLSは常染色体優性の遺伝形式をとる家族性腫瘍なので、ある大腸癌の患者さんがLSと診断されると、その方の家族にもMMR遺伝子解析を行い、もし変異が見つかれば癌を発症する前から医療介入を行うことにより早期発見・早期治療が可能になります。
当科では、LSの見逃しを一例でも減らすために消化器外科や遺伝医学部門と連携して、新たに診断された大腸癌の全ての患者さんを対象にMSI解析を行う臨床研究(universal screenig)を2017年から開始します。これにより従来法でどの程度のLS症例が見逃されているのかを明らかにし、LS診断の適切な方法を構築することが目的です。
またMSI陽性大腸癌のうちLSはおよそ1/3で、残り2/3はMLH1プロモーターのメチル化による散発性(非遺伝性)大腸癌です。散発性MSI陽性大腸癌はLSとは対照的に高齢者に多く、他にも女性に多い、右側大腸に多い、BRAF変異が高率等の特徴が知られています。Universal screeningによりLSと共に拾い上げられる散発性MSI陽性大腸癌に関しても、同時に研究を進めます。
非侵襲的な大腸がん検査法の構築
大腸がんは早期発見すれば根治が可能であります。大腸がん検診として便潜血検査は現在確立した非常に優れた検査でありますが、問題点として感度はあるが特異度がやや低いという点があります。健康診断で便潜血陽性の場合、陽性的中率が低いため全大腸内視鏡検査というのは抵抗が強く内視鏡検査を受けに来ない方が多いのが問題です。
そこで我々は便潜血検査に加えて、より特異性が高く、侵襲性を伴わないスクリーニング方法の開発を研究しております。便中DNAを用いた遺伝子解析による大腸癌スクリーニング方法の有用性について数多く報告されていますが、我々も新規同定した遺伝子解析パネルと便潜血反応やCTコロノグラフィーとの組み合わせで効率的に大腸がんを検出できることを報告してきました。
大腸腫瘍の粘膜下層浸潤メカニズムの解明
大腸上皮から発生する腫瘍では腺腫・粘膜内癌と粘膜下層に浸潤した癌ではその脈管侵襲による悪性度、予後の相違から治療法の選択が異なる。腫瘍が粘膜筋板を破壊し、浸潤する形式には病理組織学的には様々な所見が捉えられている一方で、良性腫瘍や粘膜内癌の段階にも関わらず粘膜下層へinverted growthしたり、粘膜筋板を菲薄化している病変も認められる。これら大腸腫瘍における粘膜筋板への影響に関しては未だに不明瞭ことが多く、そのメカニズムを知ることは創薬も含めて大変意義のあることと考えている。
我々はsessile serrated adenoma/polyp(SSA/P)も含めた大腸腫瘍性病変を粘膜筋板への影響の観点からそのメカニズムに関してtranslational researchにより探索を試みております。
大腸がんの腫瘍血管新生を標的とした治療方法の開発
増殖・浸潤・転移に関わる腫瘍血管新生を制御することは、がんの進行抑制のための有望な戦略と考えられています。そこで我々は腫瘍血管内皮細胞に特徴的な遺伝子異常に着目した新規血管新生阻害療法の開発を目指しております。
これまでに大腸がん組織における血管内皮細胞と正常大腸組織における血管内皮細胞の遺伝子発現の特徴を、最新のシークエンス技術を用いて明らかにしており、治療標的として有望と考えられる遺伝子を多数抽出しています。これらの遺伝子の機能解明を進めて、大腸がんの新規治療標的としての有用性を検討しております。
大腸がん発生をドライブする遺伝子異常の解明
大腸癌組織を構成する細胞は均一な集団ではなく、多様な遺伝子異常を持つ癌細胞の集合体です。このような腫瘍内不均一性は抗がん剤、分子標的薬、放射線治療抵抗性や癌再発が生じる原因として考えられています。
そこで我々は腫瘍内の細胞集団におけるゲノム異常の多様性および共通性に着目して、良性腫瘍から前がん病変や早期癌を対象として拡大内視鏡で捉えられる癌化の所見をもとに発癌の起源となる遺伝子異常を探索し、癌根本治療の標的となる遺伝子異常の同定を試みております。
大腸腫瘍の局在と遺伝子異常に関する研究
近年、大腸癌に対する抗がん剤治療がめざましい進歩を遂げているが、左側と右側結腸の癌では抗がん剤の効果に差異があるとの報告が成されている。また近年第3の発癌ルートとして大変注目されているsessile serrated adenoma/polyp(SSA/P)では右側結腸に高率に発現し、BRAF変異、CIMP-highを示すことを、我々も秋田赤十字病院消化器病センター、岩手医大分子診断病理、札幌医大分子生物学講座とのtranslational researchを通じて研究成果を発表してきたが、大腸腫瘍ではその局在により遺伝子変異の相違があることが事実として少しずつ判ってきた。しかし左側結腸にも希ながら認められるSSA/P with cytological dysplasiaでは右側結腸の同病変と遺伝子背景は全く変わらないとの指摘もあり、また左側と右側結腸は人為的に分類したに過ぎずサイエンスに基づく根拠は存在しない。
そこで我々は大腸腫瘍の局在と遺伝子異常の関連性に関して進行大腸癌も含めて、そのメカニズムの探索を試みております。
肝胆膵臓
肝胆膵臓研究
抗体を用いた新しいがん治療
肝がん、胆道がん、膵がんを対象とした新しい治療薬の開発をめざした研究を行っています。肝がん・胆道がん・膵がんはいずれもが難治性がんといわれ、残念ながら特効薬と呼べるような薬剤は見出されておりません。私たちは、これらのがん細胞に特異的に発現しているタンパク(抗原)を探索し、これに特異的に結合する抗体(モノクローナル抗体)を作成し、これを用いた抗体治療を研究しています。この抗体を用いたがん治療はすでにいくつかのがんに対して行われつつあり、その有効性が報告されています。患者さんには副作用がなく、一方、がん細胞に対して強力に効果を発揮することを期待して用いる薬剤です。私たちは、これまでも肝がんに対するFGFRという標的に対する抗体を作成し、その臨床応用を目指した研究を行ってまいりました。さらに、より安全な、そしてより強力な抗体医薬の開発を目指した研究を行っています。
発癌機序解析
肝がん、胆道がん、膵がんの遺伝子異常の検索と、これに基づく発癌機序の解析を行っています。これは、最終的にがん細胞に特徴的なタンパクや遺伝子の変化などを検出することに繋がり、より早期の診断に活用することを目指した研究を行っています。
肝がんに対する分子標的治療の最適化に関する研究
肝がんの分子標的治療薬は、現在、ソラフェニブという薬剤が最も実績のある標準治療となっていますが、どのような患者さんに効果があるかという治療効果予測は分かっておりません。われわれの多数の患者さんのデータを解析したところ、治療開始早期に出現する血圧変動が、治療効果に関わっている可能性が分かってきました。この血圧変動に関わる分子として、VEGFやeNOSなどが関わっていると考えられており、それらの分子の遺伝学的要因を検討しております。治療効果や予後が異なるいくつかの因子が同定され、現在、数を増やして検討を行っております。
抗がん剤治療による末梢神経障害の予防開発
現在切除不能・再発膵癌の標準治療の一つであるnab-paclitaxel/gemcitabine療法では、高率に副作用として末梢神経障害がおこることが知られています。この副作用によって日常生活に支障をきたし、治療継続が困難となることも少なくありません。当科では投与時の弾性ストッキング・スリーブ装着によって末梢神経障害を予防しうるか現在臨床研究を進行中です。
膵嚢胞性病変の前向き研究
膵癌のリスクファクターとして、膵癌診療ガイドライン2016年版では膵嚢胞があげられています。10㎜未満の膵嚢胞性病変が膵癌のリスクファクターであるのか、現在多施設共同前向き観察研究がおこなわれており、当科も研究分担施設として参加しています。
胆道癌の微小環境についての研究
胆道癌の浸潤・増殖、転移については他の癌種と同様、癌の微小環境が大きくかかわっていると考えられていますが、いまだ詳細は不明です。当科では癌関連線維芽細胞(cancer associated fibroblast : CAF)を中心に、これらのメカニズムを解明すべく基礎研究を進めています。
造影超音波内視鏡検査による膵腫瘍の診断研究
体外式超音波検査は、その侵襲性の低さから膵疾患診断の最初のステップと位置づけられていますが、消化管の内容物により描出困難な死角が存在します。一方、超音波内視鏡検査はこれらの障害物に妨げられることなく膵臓の詳細な観察が可能となるとともに高い空間分解能、時間分解能を有しています。2007年に肝腫瘤性病変診断目的で臨床使用認可された第二世代超音波造影剤ペルフルブタンは、低音圧の探触子を使用する超音波内視鏡検査においても造影ハーモニックイメージングが可能であり、理論上は膵疾患にも応用可能と考えられており、膵腫瘍の早期画像診断精度の向上のために、ペルフルブタンを用いた造影超音波内視鏡検査の有用性および安全性を検討しています。
研究グループ紹介
炎症性腸疾患研究グループ
当グループはグループ長である仲瀬教授の指導のもと,炎症性腸疾患,消化管免疫に関する臨床研究・基礎研究を行っている.
仲瀬教授は豊富な臨床経験と研究実績に裏打ちされた仮説を実験・検証の繰り返しで確かめること,そして「臨床に生かすこと」を目標に掲げ,臨床研究・基礎研究を主導している.さらに,厚生労働省難治性炎症性腸疾患障害に関する調査研究の班員の1人として多くのprojectを担っている.
助教である小野寺医師は教室長業務で多忙を極める中,国内外の施設との共同研究・臨床研究・治験の申請や事務局の実務を一手に引き受け,若手への研究指導も行っている.
大学院4年生である川上医師は,これまで取り組んできた「骨髄-腸管連関の解明」や「腸上皮幹細胞とニッチの再構築」に関する研究に加え,グループ長の指示する新規研究の実現にむけて奔走している.
大学院2年生である飯田医師は「腸炎関連大腸癌の発癌機序の解明」に精力的に取り組んでいる.能力の高さとガッツで既に興味深い結果を得ており,2年生ながら国内外の学会で研究成果を発表している.
臨床研究
- 家族性地中海熱遺伝子関連腸炎の診断法確立
- 炎症性腸疾患におけるMEFV遺伝子変異の検討
- CMV感染合併潰瘍性大腸炎を対象とした定量的PCR法に基づく抗ウイルス療法の適応選択と有効性に関する臨床試験
- 活動期潰瘍性大腸炎に対する漢方薬青黛の有用性
- 炎症性腸疾患患者におけるチオプリン関連副作用とNUDT15遺伝子多型との相関性に関する多施設共同研究
- 腸管型ベーチェット病におけるアダリムマブとステロイドの多施設共同前向き無作為化比較試験
- 日本潰瘍性大腸炎研究
- 炎症性腸疾患合併症とリスク因子の解析
- クローン病,潰瘍性大腸炎の小腸および大腸における薬物動態関連タンパク質の発現量解析と腸オルガノイドの薬物動態試験への有用性の評価
- 新規蛍光造影剤「ナノビーコン」を用いた炎症性発癌の体外診断
- 循環器難病に随伴する後天性フォンウィルブランド症候群の診断基準・重症度分類の確立
- 潰瘍性大腸炎粘膜治癒の定量的判定を目指した内視鏡画像解析装置の新規開発
基礎研究
- 腸上皮幹細胞とニッチの再構築
- 骨髄-腸管連関の解明
- 腸炎関連大腸癌の発癌機序の解明
- 炎症性腸疾患に対する新規治療薬の開発 など
上記の研究を仲瀬教授と共に日々精力的に行っている.研究結果を世界に先駆けて発信できるよう努めていく次第である.