| 分子・器官制御医学専攻:遺伝子医学領域 |
|
| 分子血液病態学 |
|
| スタッフ 教授 古 川 勝 久 |
|
| 限りなく再生する造血細胞の研究を通して 生命現象の本質にせまり、疾患の新たな治療へのアプローチを! |
|
| 骨髄細胞は、分化増殖して血液細胞を構成するのみならず、血管や骨など様々な器官の形成や再生に重要な働きをしている。造血幹細胞を含む骨髄細胞と、その分化増殖調節機能を分子生物学的に解明することは、生命現象の理解と血液疾患をはじめ様々な疾患の本質的な治療に直結する。 |
|
| 研究テーマ | |
| 1 造血調節機構の分子生物学的解析 2 細胞間、細胞-細胞外基質接着機構の解明 3 血球運動機序の分子生物学的解析 4 造血細胞移植時の移植片対宿主反応の解明 5 接着分子を介した抗癌剤耐性に関する細胞内シグナル伝達の解明 6 造血幹細胞とストローマ細胞のクロストーク解明 |
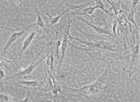 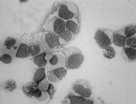 ストローマ上で分化した 不死化した骨髄 赤芽球 ストローマ細胞 |
| 研究内容の具体例 | |
| 1 血小板造血とその調節 | |
| 血小板由来TGF−βが血小板造血を負に調節し、骨髄内支持細胞由来のトロンボポエチン(TPO)とのバランスで血小板数が制御されることを初めて明らかにした(Blood 94,1961−1970, Blood 92,46−52)。ET患者の巨核芽球(血小板の幹細胞)におけるTGF−βのシグナルを調べ、Smad4(増殖抑制シグナルを核へ伝える因子)の発現が、プロモーター領域のメチレーションにより低下し、TGF−βによる負の調節からの逸脱がETの原因であることを明らかにした(Blood, 投稿中)。 | |
| 2 造血と鉄代謝 | |
| 日本人で初めて、本邦における鉄過剰症責任遺伝子である可能性が考えられるH−フェリチン遺伝子の点突然変異と、鉄沈着をもたらす機序も明らかにした(Am J Hum Genet 69,191‐197,2001)。また、血中にTfRが存在することを世界で初めて見出し、それが造血能の指標となることを明らかにしてきた。現在TfRの測定キットは全世界で広く用いられている。 | |
| 3 急性骨髄性白血病(AML)再発の機序とその克服 | |
| AML細胞がVLA分子を介してフィブロネクチンと接合し、bcl2(アポトーシス抑制因子)の発現亢進を介し、アドリアマイシン、Ara Cなどの抗癌剤に耐性となることを明らかにした。動物実験では、VLA4抗体投与により、治療効果が高まることも確認し、白血病治療に新しい戦略を開拓しつつある(Blood,投稿中)。 | |
| 4 再生医療−人工骨髄作製の試み | |
| 不可能であったヒト骨髄支持細胞(ストローマ)の不死化に成功した(Blood,投稿予定)。ストローマ上で造血幹細胞(CD34+)の増生、赤芽球の培養にも成功した。現在、人工骨髄を試験管内で作製する研究を行なっており、これまでの輸血や骨髄バンクの概念を根本から変える可能性がある(図参照)。 | |
| 5 血球運動と活性酸素 | |
| マクロファージや、好中球が、自ら産生する活性酸素により、PKCや、small G proteinを活性化し、細胞運動を促進することを見出した。炎症反応や、抗腫瘍免疫の制御に応用するべく研究中である(JBC,投稿中)。 | |
| 大学院での研究生活について |
| 研究計画の立案と、その遂行のための実技トレーニングを行う。定期的に、研究の進行状況を発表し、ディスカッションすることで、研究進行の効率化と、幅広い知識の獲得を行う。生活に必要な収入は保証される。 |
| 大学院修了後の進路 |
| 内科医としての臨床研修を終了した後は、世界の最先端の研究施設への留学を推奨している。 |