免疫制御医学部門では、免疫関連疾患の病態解明と得られた結果の臨床への応用を目指して研究を行っています。主に臨床材料から得られた免疫組織や免疫細胞を対象として、免疫システムが疾患病理にどのように関わっているのかを解析しています。特に免疫システムを調節するヘルパーT細胞の機能や、免疫応答の場を形成する上皮組織に注目して研究を進めています。
アレルギー疾患などの免疫関連疾患における、種々のヘルパーT細胞の役割を解析しています。特に濾胞ヘルパーT細胞(TFH細胞)を基軸として、検討を重ねています。抗原刺激を受けていないナイーブヘルパーT(TH0)細胞は抗原提示細胞との接触を起点として周囲のサイトカイン環境によって排他的分化を示し、TH1細胞やTH2細胞、TH17細胞、TREG細胞といった種々のエフェクターヘルパーT細胞となって機能を発揮します。エフェクターヘルパーT細胞の一種、濾胞ヘルパーT細胞(TFH細胞)はケモカイン受容体のCXCR5を発現するヘルパーT細胞サブセットとして見出されました。現在までのところTFH細胞はCXCR5やPD-1の発現多寡によりCXCR5hiTFH細胞とCXCR5loTFH細胞に分類され、両者協調してリンパ濾胞の形成を担っていることがわかっています。以前に我々は脂質メディエーターの産生に関わるアラキドン酸5−リポキシゲナーゼ(ALOX5)を欠損したマウスはTFH細胞の分化が乏しく、またTH1細胞機能に依存するIgG2aの血清レベルが常時低下していることを報告しました(AJP、2011)。ロイコトリエンを含むALOX5関連脂質メディエーターはTFH/TH1中間細胞の維持に関与している可能性が示唆されます。またIL-21レポーターマウスの研究などから炎症環境によってTFH細胞が他のエフェクターヘルパーT細胞に変容することが見出されており、TFH細胞は極めてダイナミックに自己変化を許容していることがわかります。TFH細胞を'機能的ハブ'とした免疫異常の病態があるかどうかは今後の研究が待たれますが非常に興味ある課題であり、我々はTFH細胞サブセットと病態形成に関する研究を行っています。
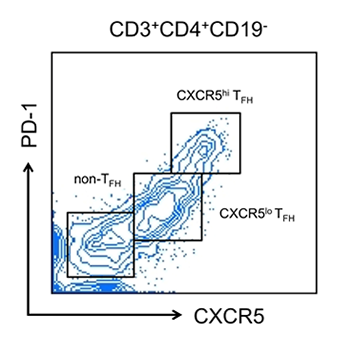
※扁桃リンパ球のFACS解析。ヘルパーT細胞(CD3+CD4+CD19-)をCXCR5とPD-1とで展開すると、CXCR5hiTFH細胞、CXCR5loTFH細胞、non-TFH細胞の3つのポピュレーションが検出される。
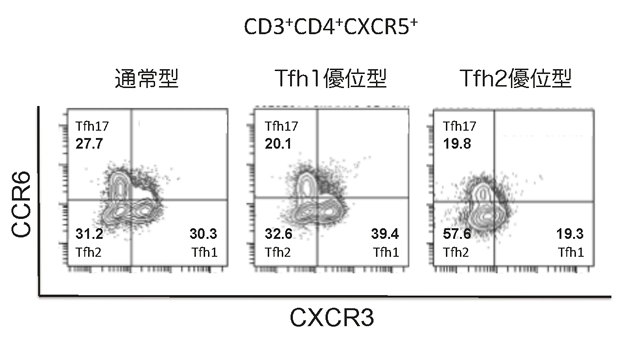
末梢血液のリンパ球の中で多数を占めるCD4+ヘルパーT細胞には血液メモリーTFH細胞(CD45RA-CD4+CXCR5+)が含まれており、それらは主に3つのポピュレーション、すなわちTFH1細胞(CXCR3+CCR6-)、TFH2細胞(CXCR3-CCR6-)、TFH17細胞(CXCR3+CCR6-)から構成されます。最近我々は免疫アレルギー疾患ではTFH2細胞が増多しており、疾患増悪に制御性B細胞(BREG細胞)が深く関与していることを明らかにしました(Clin Immunol、2015)。
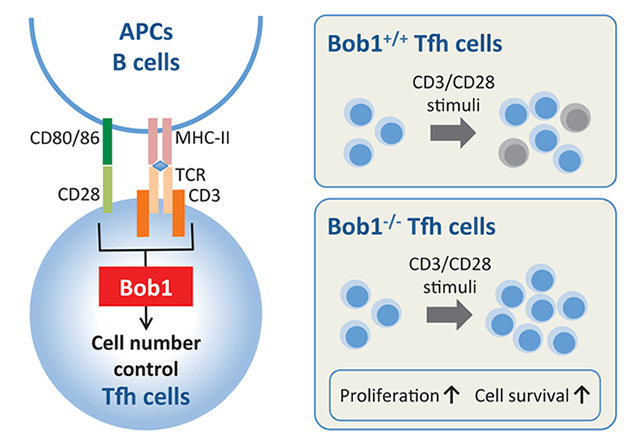
また最近、Tfh細胞の数の制御機構が抗原特異的な抗体産生のプロセスや免疫関連疾患と深い関わりがあることがわかってきました。B細胞に発現して抗原特異的な抗体産生を促す転写調節因子Bob1がヒトやマウスのTfh細胞に高発現していることを見出し、Bob1はT細胞抗原受容体やCD28の刺激に際してTfh細胞の数的調節を担っていることを報告しました(Eur J Immunol. 2016)。さらにIgG4関連疾患の病理組織を直接的に解析したところ、特殊なBCL6hiTfh細胞が病変部の形成に関与していることがわかりました(J Immunol. 2017)。
外界と内界を隔てるしくみの素地を形成する上皮細胞は、生体防御の最前線としての役割を担い、皮膚や呼吸器、消化器など多くの臓器組織を構成しています。その機能破綻は慢性炎症を惹起し、免疫アレルギー疾患などを含む様々な免疫病態に関与し、またがん化にも関連しています。エピイムノームとは上皮細胞が関わる免疫環境を示し、上皮細胞は中枢性免疫組織にも発現していることから、エピイムノームは末梢組織におけるリンパ球の機能発現はもとより、リンパ球の機能分化にも影響を及ぼしていることがわかります。上皮親和性のある転写因子群に着目して上皮細胞ネットワークの機能的意義を幅広く解析し、エピイムノームの免疫機能やその機能障害が関連する免疫病態を研究しています。具体的には、上皮細胞によるTSLPなどのサイトカインの産生機構と病態、無菌マウスを用いた食物アレルギーモデル、ヘルパーT細胞サブセットの活性化機構におけるエピイムノームの役割、などについて検討を重ねています。アトピー性皮膚炎の表皮組織ではp73アイソフォームの機能特性がTSLPの産生に影響していることを明らかにしました(J Dermatol. Sci. 2017)。
臨床病態の診断や治療を目的として、生検や手術により病変部の病理組織が検査されます。病理組織の特徴を明らかにするために様々な手法が用いられますが、一般的に顕微鏡を用いた形態解析が行われて病理組織診断がなされます。このプロセスでは、"生じていることは何か"、を明らかにしようとします。つまり、組織の特徴を形成している背景は何か、どの細胞が病態形成に関与しているのか、など様々な可能性を絞り込んでゆくことで、病理組織の特徴が浮かび上がってきます。免疫システムの組織を解析する場合も同様ですが、リンパ球を含めた免疫細胞の制御機構が解明されていないため、全体の評価が困難な場合があります。ヒト免疫システムの全体像が、まだ捉えられていないことも要因のひとつです。個々の細胞組織の性格を明らかにする還元的な研究を続けてゆくと同時に、病態を明らかにするための縁、ヒントを与えてくれる病理組織の解析も重要と考えます。病理組織の解析は、得られた実験事実の意義を検証するためにも必要不可欠です。こうした視点を忘れずに検討を重ねながら、意義ある事象を見出してゆきたいです。腫瘍の病理組織の解析の過程で、高分化型甲状腺癌にはエンドソーム輸送に関わるSNX5が高発現しており(Cancer Sci. 2012)、SNX5はTSH受容体やEGF受容体の細胞内代謝を促進して腫瘍化シグナルを抑制していることが判明しました(J Pathol. 2017)。