研究紹介
肺癌の分子病理学的研究(佐久間)
研究の背景
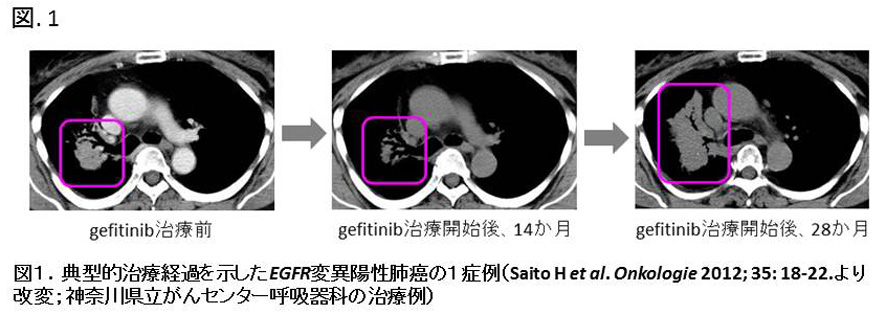
肺癌には主なものだけでも腺癌、扁平上皮癌、小細胞癌など多数の組織亜型が含まれていますが、最も発生頻度の高い亜型は腺癌です。また日本人に生じる肺腺癌の約半数には受容体型チロシンキナーゼであるepidermal growth factor receptor (EGFR) をコードするEGFR遺伝子に機能獲得性突然変異が確認されます。EGFR遺伝子変異陽性(以下EGFR mutant)肺腺癌細胞は、突然変異により恒常的に活性化したEGFR signalingに依存して生存・増殖していると考えられています。実際に変異のhot spot(突然変異の多発する遺伝子部位)であるexon 19の欠失変異や exon 21のL858R点変異が確認されたEGFR mutant肺腺癌の約7割は、EGFR tyrosine kinase inhibitors (TKIs) 治療に一旦は反応し縮小します。しかし当初EGFR TKIs治療に高感受性を示した腫瘍も一年前後でほぼ全例が治療抵抗性を獲得することが明らかにされており(図1)、EGFR TKI単剤の治療ではEGFR mutant肺腺癌を根治に導くことはできないと考えられています。現在、私はこのEGFR mutant肺腺癌細胞が示す治療抵抗性に焦点を当てた研究を行っていますが、ここでは多数の共同研究者の先生方とともに私が展開してきた研究を新しいものから過去に遡るように紹介します。
研究紹介
1)癌細胞の上皮間葉転換 epithelial to mesenchymal transition (EMT)がもたらすEGFR TKI治療抵抗性機構の解明
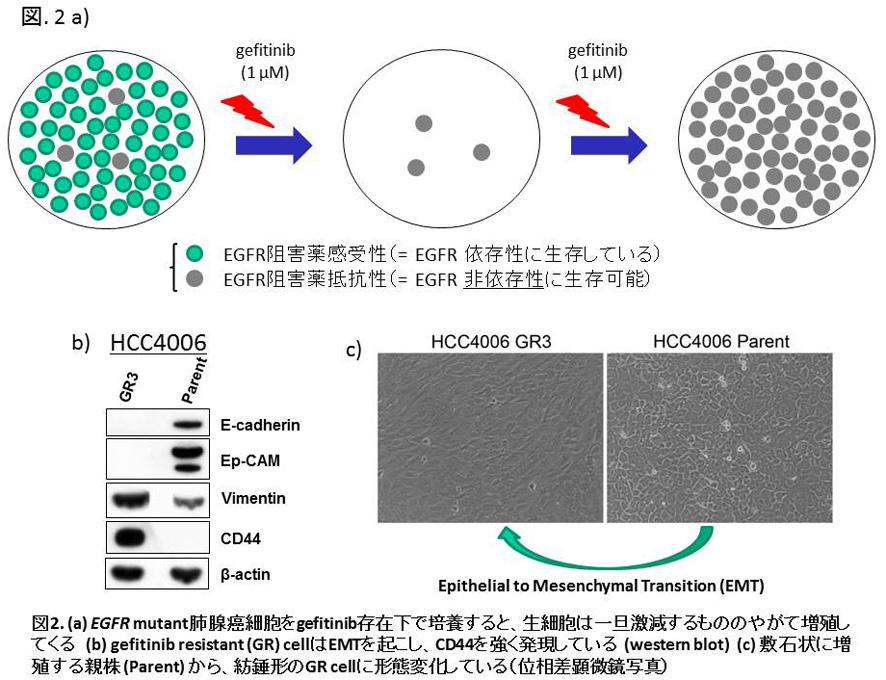
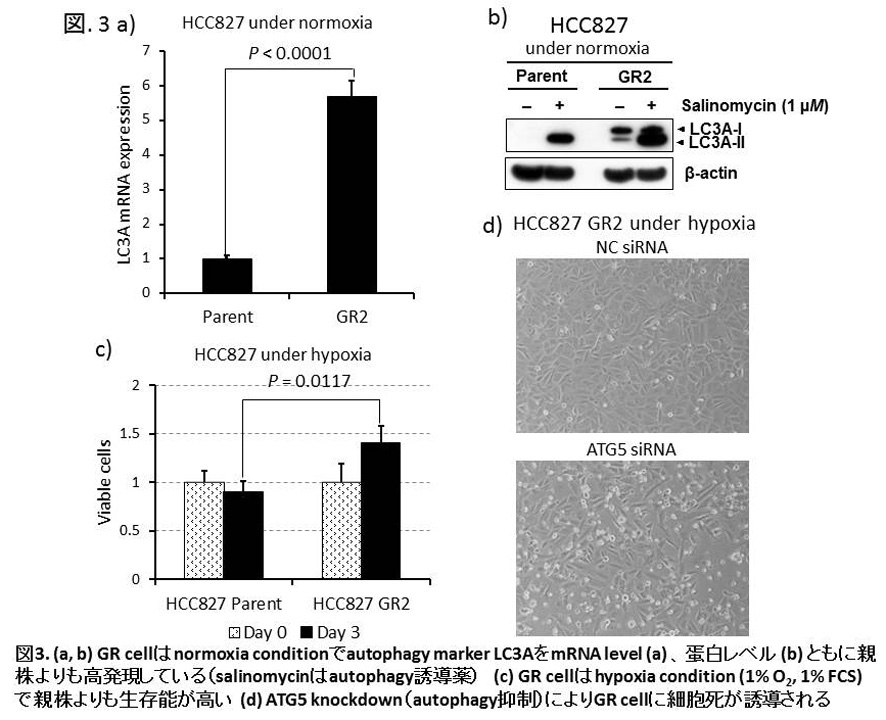
EGFR遺伝子exon 19に欠失変異を有し、EGFR TKIs治療に高感受性を示す2つの肺腺癌細胞株HCC827, HCC4006をEGFR TKIであるgefitinib存在下で培養すると、多くの癌細胞はapoptosisに陥りますが、必ず少数の細胞が生き残り、それらがやがて増殖してきます(図2a)。この過程は上記したEGFR TKI治療の臨床経過を見事に模倣しています。我々はgefitinib存在下でも増殖可能な細胞をgefitinib resistant (GR) cellと命名しましたが、GR cellは上皮間葉転換 (epithelial to mesenchymal transition, EMT) を起こし、EGFR signaling非依存性に生存・増殖可能な細胞でした(図2b, c)。GR cellはEGFR TKIsで細胞死に誘導することはできないことから、治療標的となりうるEGFRシグナル経路以外の分子機構の有無を探索しました。その結果、GR cellはその親株と比較するとautophagy活動レベルが高く(図3a, b)、低酸素・低血清環境という癌組織中心部を模倣した環境下での生存力が親株よりも有意に高いことが分かりました(図3c)。Autophagy関連分子であるATG5やBeclin1の発現をsiRNAで抑制すると、GR cellのviabilityは低酸素・低血清環境下で著しく減少することも確認しました(図3d)。以上の結果は、GR cellはEGFR阻害薬抵抗性を示すのみならず、その高いautophagy能に依存しながら低酸素・低血清という厳しい生存環境に適応していることを示唆しています。EGFR TKI抵抗性獲得後の肺癌組織の解析は残念ながら行うことができませんでしたが、未治療のEGFR mutant肺腺癌組織の一部の癌細胞にはautophagosomeが実際に形成されていることは確認できました。よってautophagyが活発に生じたEGFR mutant肺腺癌細胞がEGFR TKI治療に抵抗性を示すことが示唆されました (Sakuma et al. Lab Invest 2013)。
2)癌細胞と細胞外基質との接着がもたらすEGFR TKI治療抵抗性機構の解明
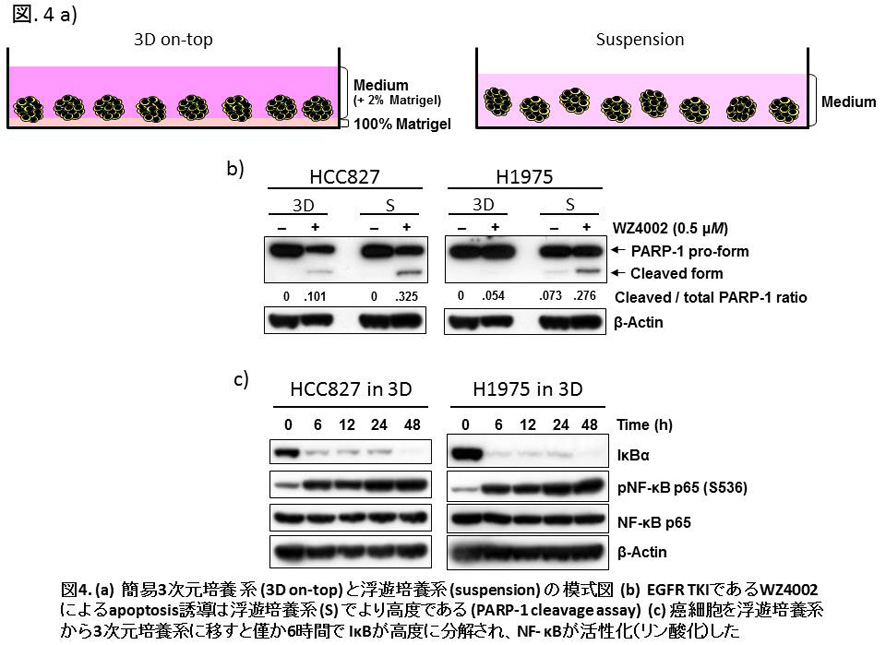
EGFR mutant肺腺癌細胞は、浮遊培養系(脈管内や胸水中に浮遊する癌細胞のin vitro model)ではEGFR TKIs に対して高感受性を示し容易にapoptosisに陥るのに対し、通常の単層接着培養系で維持された場合、その癌細胞が発現するEGFRの自己リン酸化(活性化)は浮遊状態と同様にEGFR TKIsによりほぼ完全に抑制されるにもかかわらず、EGFR TKIsが誘導するapoptosisに顕著に抵抗性を示すという興味深い現象を見出しました (Sakuma et al. Lab Invest 2012)。生体内においても周囲の細胞外基質と接着するEGFR mutant肺腺癌細胞が浮遊細胞よりもEGFR TKIs治療に抵抗性を示すか否かを検証するために、我々はin vivoの環境により近いと想定されるMatrigel(EHS肉腫細胞が産生する細胞外基質)を用いた3次元培養系を導入しました(図4a)。3次元培養系で維持されたEGFR mutant肺腺癌細胞は、浮遊培養された癌細胞と比較するとEGFR TKIであるWZ4002が誘導するapoptosisに抵抗性であることが確認されました(図4b)。その機序を探索したところ、浮遊状態から3次元環境に癌細胞を移すと僅か6時間でNF-κBを抑制するIκBの発現が激減し、NF-κB subunitであるp65が活性化することを見出しました(図4c)。さらにNF-κB signalingを阻害する小分子治療薬 TPCA-1を併用すると3次元培養された肺腺癌細胞のEGFR TKIへの感受性は顕著に増加することも確認しました。よって3次元培養系で維持されたEGFR mutant肺腺癌細胞が示すapoptosis抵抗性には、3次元培養状態でのみで確認されるNF-κB signalingの亢進が一定の役割を果たしていると考えられました (Sakuma et al. Biochem Biophys Res Commun 2012)。
3)小型肺腺癌の術後再発を規定する病理組織学的因子とその分子機構の解明
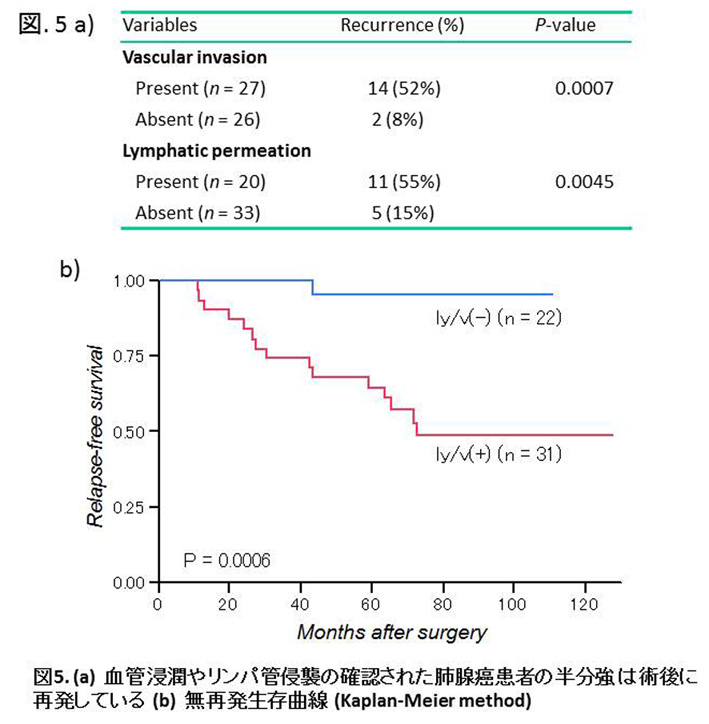
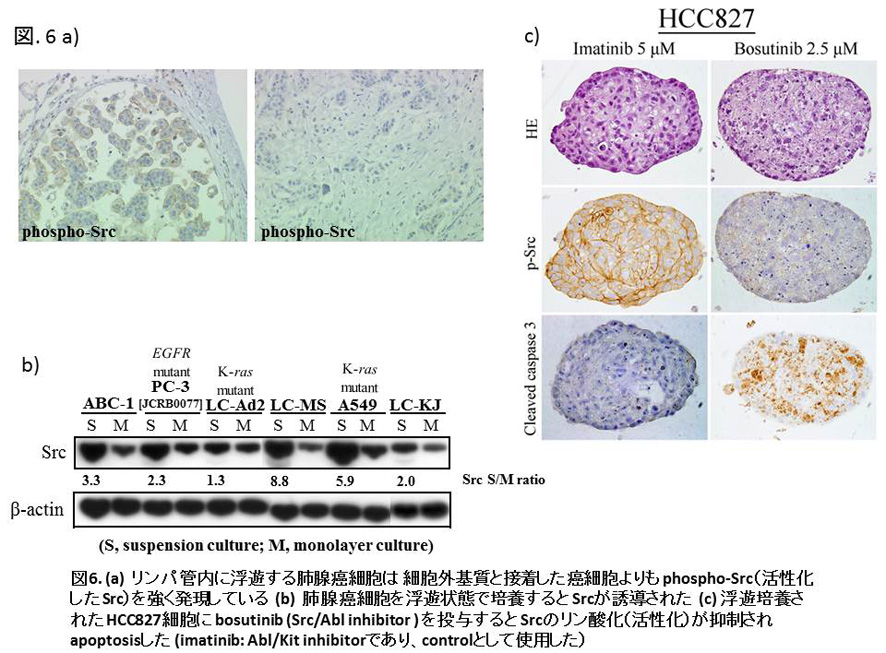
標準手術(肺葉切除+リンパ節郭清)を受け、病理病期IA期の早期肺腺癌と診断された患者さんの約8割は手術で完治するものの、約2割は再発し死に至ることが知られています。私たちがこの研究を開始した当時は、外科的切除のみで治癒する一群(低悪性度群)の画像診断上および病理組織学的特徴は既に明らかにされていました。しかし、標準的外科手術を受けても再発する群(高悪性度群)の病理学的特徴は必ずしも明確ではありませんでした。術後に再発した群と再発のない群とで様々な病理組織学的因子やEGFRやKras遺伝子変異の有無等を比較検討したところ、脈管侵襲(血管やリンパ管への癌細胞の浸潤)の有無と術後再発(その殆どは遠隔転移再発)の有無は有意に相関していました (Sakuma et al. Lung Cancer 2009) (図5a, b)。本来、正常な上皮細胞は細胞外基質から遊離するとアポトーシスに陥る(この現象はanoikisと呼ばれる)のに対し、癌細胞は細胞外基質から遊離してもアポトーシスには陥らない(anoikis抵抗性を示す)ため、脈管内に浸潤し浮遊する癌細胞もアポトーシスせず、やがて一部の癌細胞が他臓器に生着し、転移巣を形成すると考えられています。anoikis抵抗性の獲得は癌の転移が成立するための必須の分子機構の一つであるため、原発性肺腺癌組織と肺腺癌細胞株を使いanoikis抵抗性の分子機構を解析しました。その主な結果として、1)肺組織内のリンパ管内で浮遊した肺腺癌細胞は、付着した癌細胞と比較するとリン酸化(活性型)Src を強く発現すること(図6a)2)肺腺癌細胞株を浮遊培養系で培養すると全ての細胞株で Srcが誘導されること(図6b)(3)浮遊培養された肺腺癌細胞株にSrc TKIを投与するとアポトーシスが誘導されること(図6c)が確認されました。以上の結果から脈管内や胸水中で浮遊した状態で存在する肺腺癌細胞の治療薬としてSrc阻害薬が有効であることが示唆されました (Sakuma et al. J Pathol 2010)。
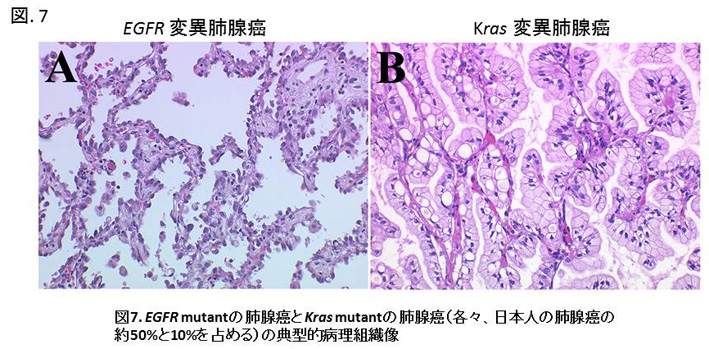
4)肺腺癌の分子分類と病理組織像との相関
肺腺癌は個々の腫瘍間にも、また同一の腫瘍内でも非常に多彩な組織像を呈することが知られています。私たちの以前の検討でもEGFR mutantとKras mutantの肺腺癌の典型的病理組織像は全く異なっていることを確認しています(Sakuma et al. Am J Pathol 2007) (図7)。その後、同定されたEML4-ALK融合遺伝子陽性の肺腺癌の多くも特徴的な組織像を呈することが知られています。より重要なことはこれらのdriver mutationの相違により臨床経過や投与すべき有効な薬剤(分子標的薬)が異なるということです。よって同じ肺腺癌と病理学組織学的に分類される腫瘍には多彩な、根本的に別個の腫瘍群から構成されていると考えられています。