神経再生医療グループ
我々は、本学神経再生医療学部門と共同で、難治性疾患に対する幹細胞を用いた再生医療の実現を目指し、日々基礎研究を行っております。現在臨床試験が終了した「急性期脊髄損傷に対する自己骨髄幹細胞移植治療」の 一般医療化に主軸を置きつつ、障害された脊髄の可塑性や再生に関する研究、各種脳脊髄疾患への臨床研究、細胞治療の効果判定の為の新しい方法の開発研究などを精力的に行っています。
脊髄損傷に対する細胞移植研究
脊髄損傷、脳梗塞などの難治性神経疾患に対する骨髄幹細胞の移植が、機能回復をもたらすことが様々な基礎的研究から明らかになっています。移植した骨髄幹細胞が損傷神経組織に与える詳細なメカニズムを解明し、来るべき臨床応用に向けた、理論的根拠を構築しています。 また、適切な神経再生療法の確立に向け、様々な神経損傷動物モデル(脊髄損傷モデル、海綿体神経損傷モデル、脳性麻痺モデル、てんかんモデルなど)に対して骨髄幹細胞を含む多種の幹細胞移植を試みています。
特に、脊髄損傷の知見として、急性期損傷に加え、損傷から時間の経過した慢性期損傷モデルラットにおいて、骨髄間葉系幹細胞を投することで、投与翌週から行動学的改善が認められたことを報告しています(図 1)。また、そのメカニズムとして血液脊髄関門の修復、微小血管の再構築、脱髄軸索の再有髄化(図 2-4)を報告しています。
特に、脊髄損傷の知見として、急性期損傷に加え、損傷から時間の経過した慢性期損傷モデルラットにおいて、骨髄間葉系幹細胞を投することで、投与翌週から行動学的改善が認められたことを報告しています(図 1)。また、そのメカニズムとして血液脊髄関門の修復、微小血管の再構築、脱髄軸索の再有髄化(図 2-4)を報告しています。
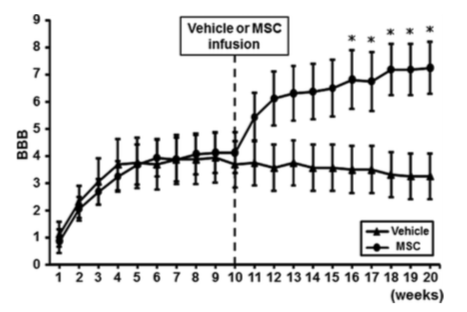
慢性期脊髄損傷の実験的動物モデルに対するMSC移植後の運動機能の改善(BBB score)
損傷後下肢の運動はある程度自然回復を認めたが6週前後でプラトーに達した。MSCの経静脈的投与を行ったところ、移植後1週から後枝の痲痺の改善を認めた。
(Morita T et al Neurosicence 2016)
(Morita T et al Neurosicence 2016)
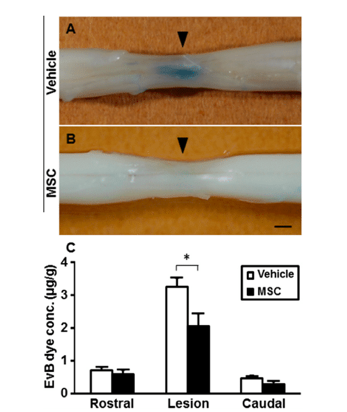
移植後1周のラットにEvans Blueを静脈内投与した。MSC群は損傷部において漏出量が有意に小さく、血液脊髄関門の機能改善が示唆された。
(Morita T et al Neurosicence 2016)
(Morita T et al Neurosicence 2016)
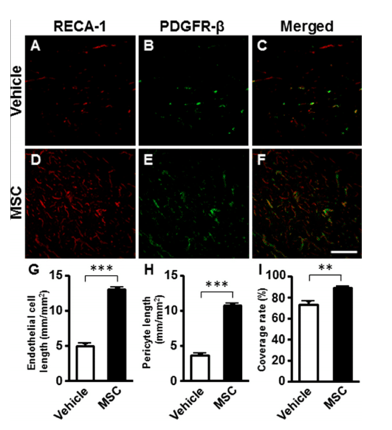
血管内皮細胞、周皮細胞の免疫組織学的解析
MSC群は内皮細胞に対する周皮細胞の被覆率が高く、微小血管系の再構築が起きていると考えられる。
(Morita T et al Neurosicence 2016)
(Morita T et al Neurosicence 2016)
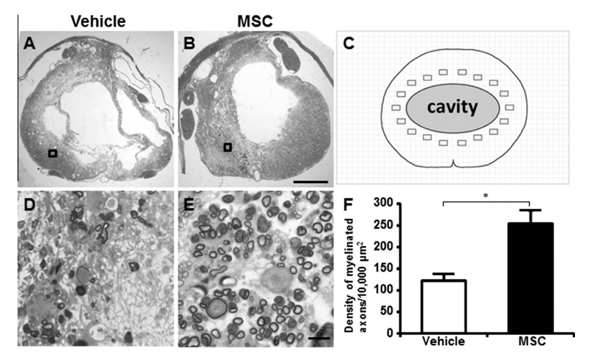
損傷20週後の脊髄損傷部トルイジンブルー染色
MSCでは脱髄軸索の再有髄化率が有意に高かった。
(Morita T et al Neurosicence 2016)
(Morita T et al Neurosicence 2016)

バイオメカニクスグループ
バイオメカニクスグループでは、主に未固定凍結人体標本を使用して運動器の機能解剖や動的解析を行っています。具体的には、(1)電磁気センサーを用いた三次元動態評価、(2)ロボットシステムを用いた関節運動評価、を行っています。
(1)電磁気センサーを用いた三次元動態評価
電磁気センサーを用いて三次元的に空間位置座標を計測することにより、これまで腓骨の運動、足関節遠位脛腓靭帯の機能および治療、後脛骨筋機能不全に対する治療など様々な研究を行っています。
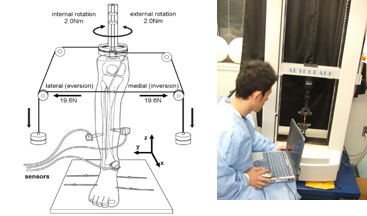
(2)ロボットシステムを用いた関節運動評価
首都大学東京との共同研究によって、精密な6自由度ロボットシステムを用いて前十字靱帯の力学的特性や靭帯再建術、足関節外側靭帯の力学的特性や手術治療法、人工膝関節置換術の術式や機種の違いによる評価、など様々な研究を行っています。

骨軟部腫瘍グループ



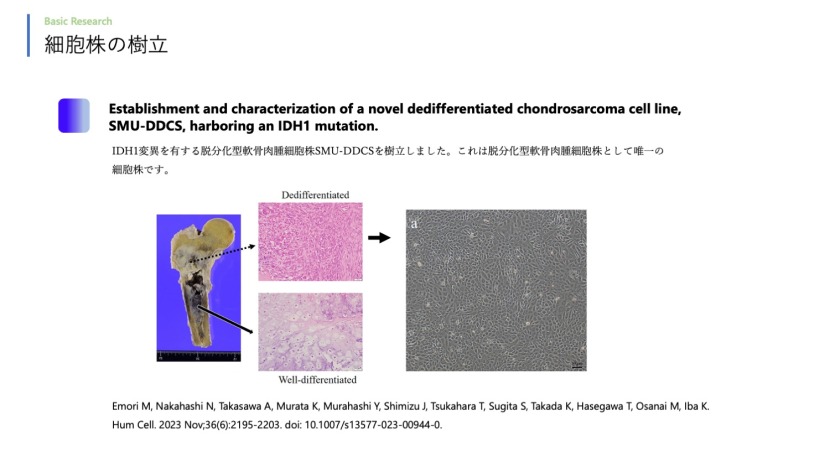
細胞生理学・疼痛グループ
私達は主に電気生理学的手法を用いて、椎間関節や椎間板などの脊椎構成要素、肩関節、足関節などにおける機械的感覚受容器の分布や生理学的特性についての研究を行ってきました。感覚受容器はその生理学的特性により、固有感覚受容器と侵害受容器に分けられます。固有感覚受容器の研究は、脊柱や四肢の関節の運動制御システムの解明、障害の予防やパフォーマンス向上といったスポーツ医学の領域に応用されてきました。一方、侵害受容器の研究では、痛みの受容や伝達機構の一端を明らかにしこれまで報告してきました。
脊椎疾患で多くみられる神経障害性疼痛に関して、その発生・伝達メカニズムを解明するべく、in vivo patch-clamp法を用いて痛みの伝達機構に重要とされる脊髄後角での微小シナプス伝達を解析したり(Terashima Y et al., PAIN 2011, Miyakawa T et al., Mol Pain 2014)、後根神経節細胞での痛みに関わる受容体の発現や電気生理学的特性の解析を行っています。また交感神経が痛みに関与している可能性が示唆されており(Tanimoto K et al.,Clin Orthop Relat Res 2011, Iwase T et al., Bone Joint Res 2012)、治療への応用を検討しています。
また最新のMRI撮影技術を用いてこれまで困難であった疼痛発生部位の詳細な解析を行い、痛みの診断に役立つツールへの応用を目指して研究をすすめています(Takebayashi T et al., Open J Radiology 2012, Takashima H et al., Skeletal Radiol 2012, Spine 2013)。
さらに脊椎疾患で多くみられる神経障害性疼痛に関して、その発生・伝達メカニズムを解明するべく、ラット神経根絞扼モデルを用いて痛みの解析をしています。後根神経節における交感神経の発芽やアドレナリンα2受容体に増加など交感神経系が疼痛に関与し、交感神経切除やα2-antagonistが神経障害性疼痛を抑制する可能性について報告し(Ogon I et al., Spine 2015, Ogon I et al., Eur J Pain 2016, Ogon I et al., Spine 2018)、治療への応用を検討しています。これらの研究は将来的に難治性とされる慢性疼痛に対する治療に役立つものであると考えています。
近年は関節軟骨の疼痛機序に関しての研究を行っています。ラット変形性足関節症モデルを作成(Jimbo S et al., J Arthritis 2017 )し、ヒアルロン酸ナトリウムの効果の検討を行ってきました。現在はin vivo patch-clamp法を用いて脊髄後角での微小シナプス伝達を解析し、電気生理学的に足関節の疼痛機序について研究を行っています。
脊椎疾患で多くみられる神経障害性疼痛に関して、その発生・伝達メカニズムを解明するべく、in vivo patch-clamp法を用いて痛みの伝達機構に重要とされる脊髄後角での微小シナプス伝達を解析したり(Terashima Y et al., PAIN 2011, Miyakawa T et al., Mol Pain 2014)、後根神経節細胞での痛みに関わる受容体の発現や電気生理学的特性の解析を行っています。また交感神経が痛みに関与している可能性が示唆されており(Tanimoto K et al.,Clin Orthop Relat Res 2011, Iwase T et al., Bone Joint Res 2012)、治療への応用を検討しています。
また最新のMRI撮影技術を用いてこれまで困難であった疼痛発生部位の詳細な解析を行い、痛みの診断に役立つツールへの応用を目指して研究をすすめています(Takebayashi T et al., Open J Radiology 2012, Takashima H et al., Skeletal Radiol 2012, Spine 2013)。
さらに脊椎疾患で多くみられる神経障害性疼痛に関して、その発生・伝達メカニズムを解明するべく、ラット神経根絞扼モデルを用いて痛みの解析をしています。後根神経節における交感神経の発芽やアドレナリンα2受容体に増加など交感神経系が疼痛に関与し、交感神経切除やα2-antagonistが神経障害性疼痛を抑制する可能性について報告し(Ogon I et al., Spine 2015, Ogon I et al., Eur J Pain 2016, Ogon I et al., Spine 2018)、治療への応用を検討しています。これらの研究は将来的に難治性とされる慢性疼痛に対する治療に役立つものであると考えています。
近年は関節軟骨の疼痛機序に関しての研究を行っています。ラット変形性足関節症モデルを作成(Jimbo S et al., J Arthritis 2017 )し、ヒアルロン酸ナトリウムの効果の検討を行ってきました。現在はin vivo patch-clamp法を用いて脊髄後角での微小シナプス伝達を解析し、電気生理学的に足関節の疼痛機序について研究を行っています。