研究紹介
第三世代EGFR TKI耐性の分子機構を報告
研究の背景
日本人に生じる肺腺癌の約半数には受容体型チロシンキナーゼであるepidermal growth factor receptor (EGFR) をコードするEGFR遺伝子に機能獲得性突然変異が確認されます。EGFR遺伝子変異陽性(以下EGFR mutant)肺腺癌細胞は、変異により恒常的に活性化したEGFR signalingに依存して生存・増殖していると考えられており、実際に変異のhot spot(突然変異の多発する遺伝子部位)であるexon 19の欠失変異や exon 21のL858R点変異が確認されたEGFR mutant肺腺癌の70–80%は、EGFR tyrosine kinase inhibitors (TKIs) 治療に一旦は反応し縮小します。しかし当初EGFR TKI治療に高感受性を示した腫瘍も一年前後でほぼ全例が薬剤抵抗性を獲得することが明らかにされています。その最大の原因(約半数に同定される)は第二のEGFR遺伝子変異 T790Mであること知られています。変異が一つの際は変異型EGFR蛋白のキナーゼ活性を抑制できたgefitinibやerlotinibも2個目の変異が加わり、構造が変化した変異型EGFRのキナーゼ活性は抑制できないことが知られています。しかしL858R + T790Mやexon 19 deletion + T790Mを有する変異型EGFRでさえも抑制可能な“第三世代”EGFR TKIは既に複数開発され、臨床試験が進んでいます。これらの新薬が一定の治療効果を示すことは明らかですが、単剤でEGFR mutant肺腺癌を完治させることは依然としてできません。第三世代EGFR TKIへの獲得耐性の機序(分子機構)は十分に検索されていないため以下の研究を行い論文発表しました。
研究紹介
- 異性化酵素Pin1がEGFR TKI抵抗性に関与しうることを報告 (Sakuma et al. Lab Invest 2016; 96: 391-8.)
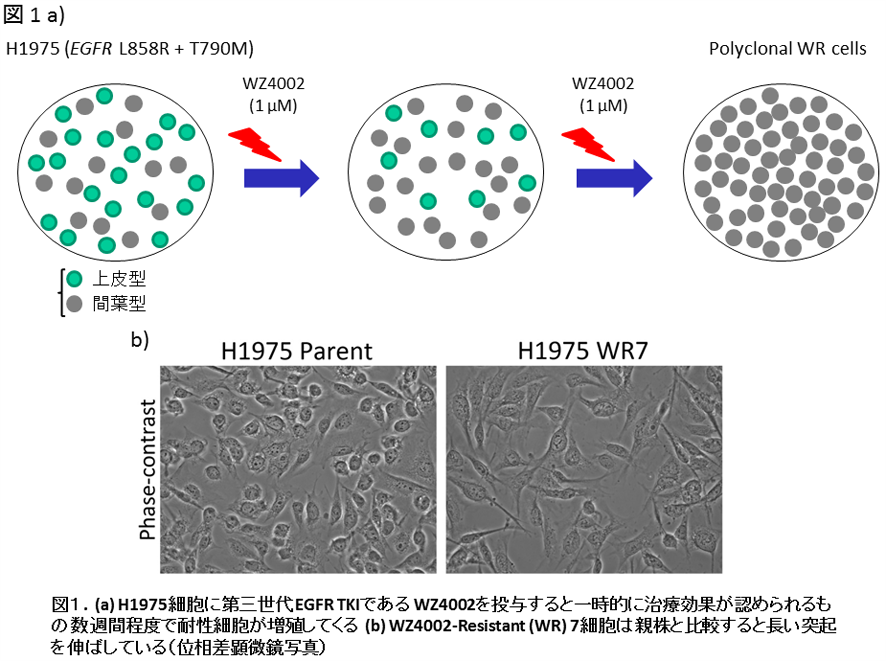
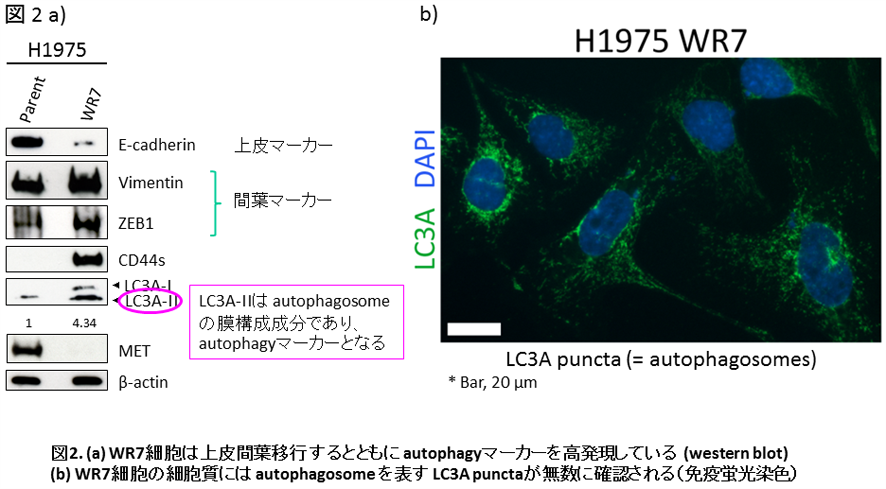
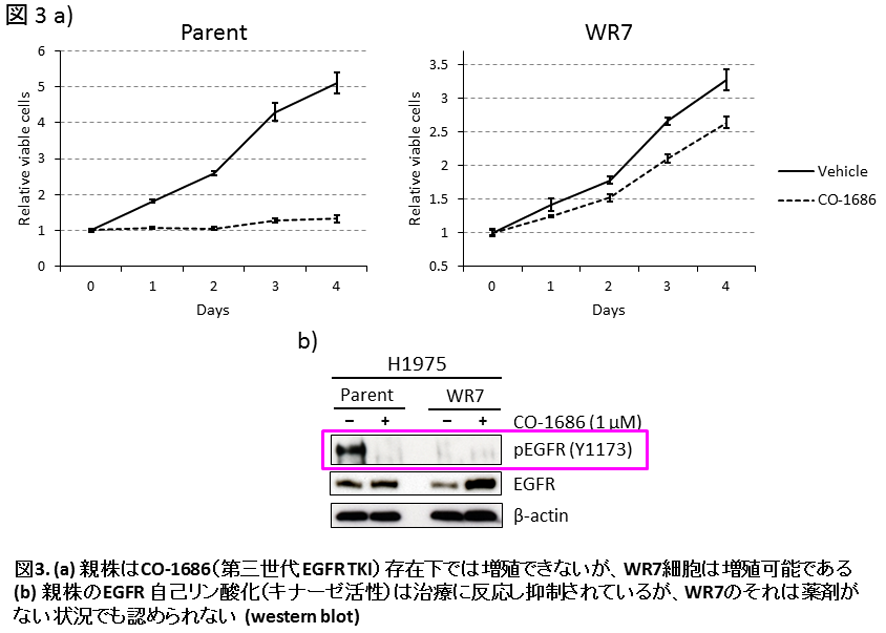
H1975と名付けられたEGFR mutant肺腺癌細胞株はEGFR遺伝子にL858R + T790Mの変異が存在することが知られています。よってこの細胞株に対してはgefitinibやerlotinibは無効です。期待の新薬である第三世代EGFR TKIの一つWZ4002で数週間ほど治療すると早くも薬剤耐性細胞が増殖してきます(図1a)。薬剤耐性細胞をcloningし親株と形態を比較すると、WR (WZ4002 Resistant) 7細胞でより長い突起を伸ばしていることが明瞭です(図1b)。上皮マーカー、間葉マーカーの発現をwestern blot法で確認すると、WR7 cellは上皮間葉移行 (epithelial to mesenchymal transition, EMT) を起こしていることが確認されました(図2a)。同時にこのWR7細胞ではautophagyが活発に生じていることも分かりました(図2a, b)。このautophagyの活性化は以前に詳細に解析した別のEGFR mutant肺腺癌細胞株であるHCC827やHCC4006から樹立されたEGFR TKI耐性細胞と同様と言えます(Sakuma et al. Lab Invest 2013; 93: 1137-46.)。今回樹立したH1975 WR7細胞もautophagy依存性に生存していることも確認しています (data not shown)。H1975 WR7細胞はその親株と異なり、もう一つの第三世代EGFR TKIであるCO-1686存在下でも増殖可能であり、かつ興味深いことに薬剤で治療していない状態でもEGFRの自己リン酸化(活性化)は確認できませんでした(図3a, b)。以上の実験結果はH1975 WR7細胞ではEGFRへの依存性が低く、代償的にautophagy依存性が高い細胞であることを示唆しています。
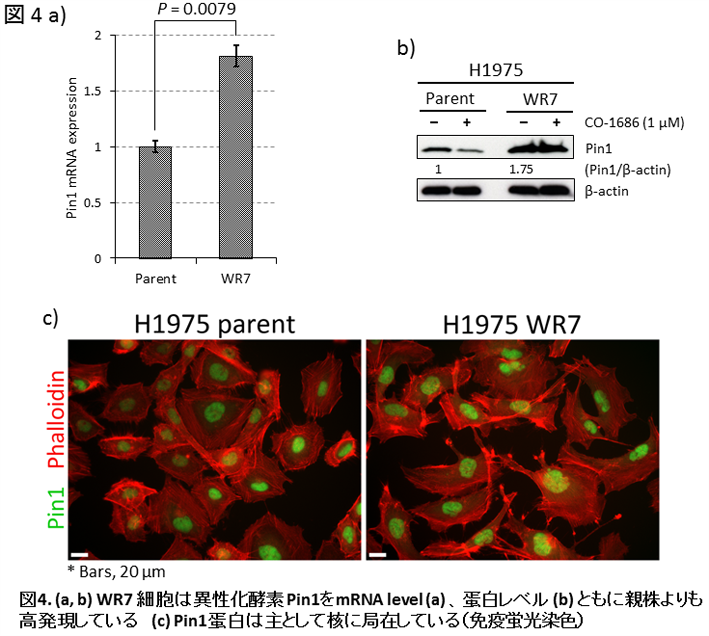
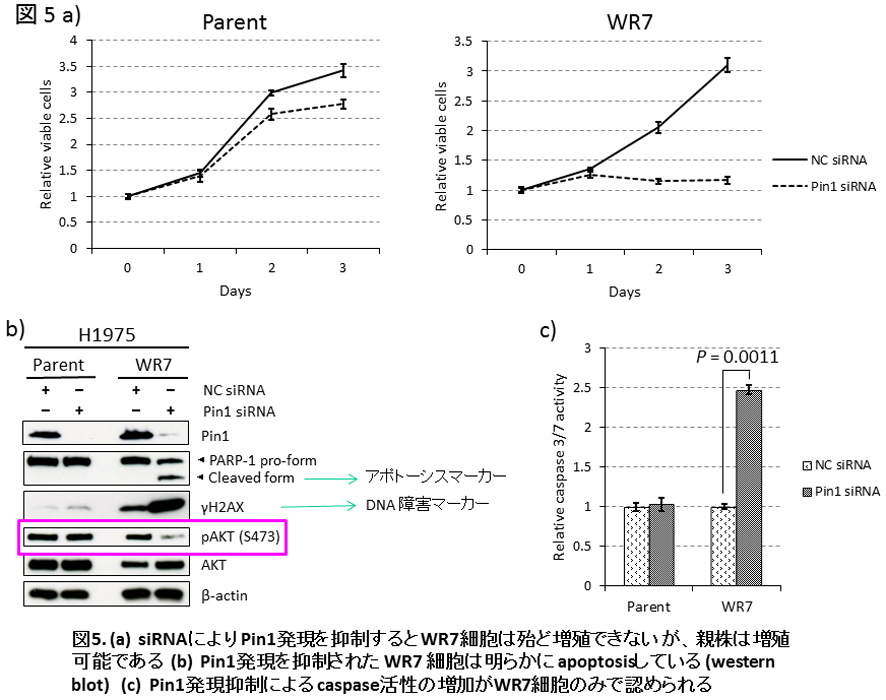
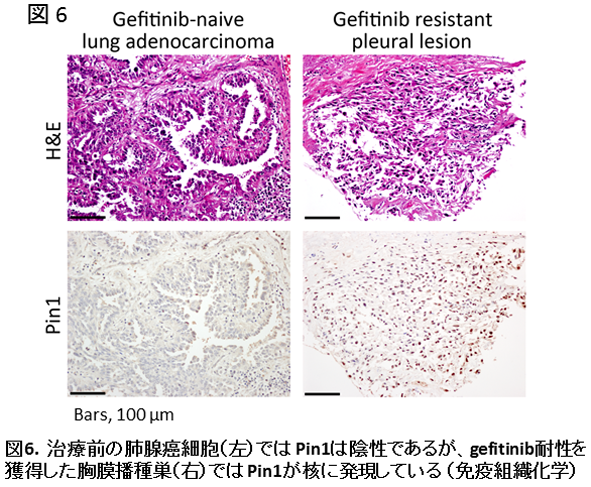
今回着目したPin1は異性化酵素でありリン酸化されたserine/threonine kinaseの立体構造をcis体あるいはtrans体に変換する働きを持ちます。蛋白の立体構造はその機能と直接的に関連することから、Pin1は細胞内に数多く存在するserine/threonine kinaseの機能を調節していると考えられます。先行する研究ではiPS細胞を含む(正常)幹細胞やいわゆる癌幹細胞の生存を促進すると報告されている分子です。今回、我々が検索したところPin1はmRNA、蛋白ともに親株よりもWR7細胞に多く発現していました(図4a, b)。またPin1は主として核に局在していることも分かりました(図4b)。次いで親株、WR7細胞で発現するPin1をsiRNA導入により抑制すると、親株には顕著な変化を認めないものの、WR7細胞では増殖が顕著に抑制され(図5a)、かつapoptosisが生じていることが分かりました(図5b, c)。Pin1 knockdownがWR7細胞にapoptosisをもたらす詳細な機序は不明ですが、WR7細胞のみでAKTのリン酸化が抑制されていることから(図5b)、これが原因の一つと考えられます。さらに本学附属病院で治療されたEGFR mutant肺腺癌のお一人の患者さんのTKI治療前と治療後(耐性獲得後)の癌組織を解析したところ、高分化乳頭状腺癌である治療前の組織ではPin1は陰性ですが、耐性獲得後のEMTを生じた胸膜播種巣ではPin1が核に発現していました(図6)。以上の培養細胞を使用した詳細な実験とそれを裏付けるような臨床検体でのPin1発現状態から、Pin1はEGFR TKI耐性に関与している可能性が示唆されました。